Mechanismus für Schäden durch Röntgenstrahlung identifiziert
Heidelberger Wissenschaftler untersuchen elektronische Zerfallsprozesse mit Hilfe der Quantenchemie
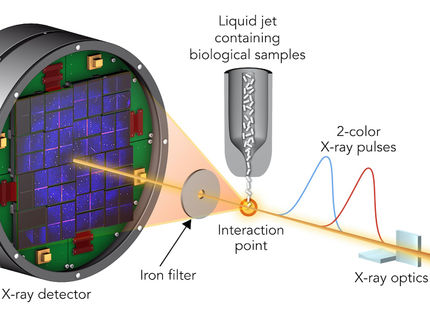
Welche Vorgänge laufen im Detail ab, wenn Röntgenstrahlung an Biomolekülen mit einem Metallzentrum Strahlenschäden verursacht? Dieser Frage ist ein Wissenschaftlerteam am Physikalisch-Chemischen Institut der Universität Heidelberg nachgegangen. Die Forscher haben dazu die zugrundeliegenden elektronischen Zerfallsprozesse, die durch Absorption der Röntgenstrahlung ausgelöst werden, mit quantenchemischen Methoden untersucht. Dabei hat sich gezeigt, dass das Metallzentrum eine entscheidende Rolle bei der Zerstörung des Moleküls spielt.
Strahlenschäden, die aus der Wechselwirkung von hochenergetischer Röntgenstrahlung mit biologischer Materie entstehen, stellen ein in der Wissenschaft allgemein bekanntes Phänomen dar. Sie treten unter anderem auf, wenn Substrate – wie etwa Proteine – mit Hilfe von Röntgenlicht mit dem Ziel analysiert werden, die elektronische Struktur oder die räumliche Anordnung der Atome zu bestimmen. Diese Schäden zeigen sich verstärkt, so Prof. Dr. Lorenz S. Cederbaum, in unmittelbarer Umgebung von Metallzentren, die essentiell für die Stabilität und biologische Funktion der Biomoleküle sind.
Die elektronischen Zerfallsprozesse, die damit verbunden sind, haben die Heidelberger Forscher mit Hilfe computergestützter Methoden aus der Quantenchemie untersucht. Im Mittelpunkt standen dabei die Vorgänge, die ablaufen, wenn Röntgenstrahlung durch das Metallzentrum eines Biomoleküls absorbiert – also sozusagen aufgesogen – wird. Als Modellsystem nutzten die Wissenschaftler ein sogenanntes Microcluster. Dabei handelte es sich um ein chemisches System, bei dem Wassermoleküle um ein Metallzentrum – hier das zweifach positiv geladene Magnesiumion – angeordnet sind.
Wie Prof. Cederbaum erläutert, verliert das Metallzentrum durch die Absorption von Röntgenstrahlung zunächst mehrere Elektronen. Dadurch entsteht ein hochgeladenes und hochenergetisches Metallion, das anschließend durch eine Kaskade von elektronischen Zerfallsschritten in seinen ursprünglichen Zustand zurückkehrt. Bei einigen dieser Schritte wird Energie vom Metallzentrum auf die Nachbarmoleküle übertragen – ein Vorgang, der als Interatomic Coulombic Decay (ICD) bezeichnet wird; bei anderen Zerfallschritten, dem sogenannten Electron Transfer Mediated Decay (ETMD), gehen Elektronen der benachbarten Moleküle auf das Metallion über.
Beide Prozesse sind nach den Worten von Prof. Cederbaum ultraschnell und laufen auf einer Skala von Femtosekunden – dem tausendmillionsten Teil einer Mikrosekunde – ab. Sie lassen damit nur extrem wenig Zeit für die Bestimmung der genauen Molekularstruktur. Im Laufe der Zerfallskaskade geben mehrere Nachbarmoleküle sowohl durch ICD- als auch durch ETMD-Prozesse langsame Elektronen ab. Die Moleküle laden sich also positiv auf, was zu einem Auseinanderbrechen des Microclusters führt.
In einem größeren System, etwa einem Protein mit einem Metallzentrum, würden die positiv geladenen Nachbarmoleküle und die langsamen Elektronen mit dem Biomolekül reagieren und weitere Sekundärschäden anrichten, wie Prof. Cederbaum erläutert. Das Metallzentrum wirkt somit wie eine Linse, die die Energie des Röntgenlichts auf die unmittelbare Umgebung fokussiert. Dadurch wird die umgebende chemische Struktur auf einer schnellen Zeitskala massiv verändert.
„Wir gehen davon aus, dass der von uns identifizierte Mechanismus eine wichtige Rolle für Strahlenschäden in biologischen Bausteinen mit Metallatomen spielt, darunter vor allem Proteine und die DNA“, sagt Prof. Cederbaum. Die Wissenschaftler hoffen, dass diese Erkenntnisse einen Beitrag leisten zur Entschlüsselung der komplizierten Prozesse, die in lebenden Organismen durch Röntgenstrahlung ausgelöst werden.
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für Biotechnologie, Pharma und Life Sciences bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.