Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 11116 Beiträge für Sie gefunden
-
Validierung der aseptischen Abfüllung mittels MF
Rubrik: Biotechnologie
(Treffer aus TechnoPharm, Nr. 02, Seite 100 (2017))
Validierung der aseptischen Abfüllung mittels MF / Teil 2 * Teil 1 des Beitrags ist erschienen in TechnoPharm 7, Nr. 1, 38–43 (2017). · Berchtold M · Novartis Pharma Stein AG, Stein (Schweiz)
Der an einer aseptischen Abfüllung beteiligte Mitarbeiter stellt – speziell im konventionellen Reinraum (Zone A mit Hintergrund Zone B) – das größte Risiko für die mikrobiologische Qualität eines aseptisch abgefüllten Sterilproduktes dar. Daher ist sowohl seine bloße Anwesenheit (s. Kap. 5.7) als auch speziell jede seiner mit der aseptischen Abfüllung zusammenhängende Tätigkeit im Reinraum via MF abzudecken. Dies gilt speziell für diejenigen A-Zonen-Eingriffe, die ein direktes Risiko für die Produktsterilität darstellen können, also z. B. alle Eingriffe, die ein Öffnen/Schließen einer sterilen Schlauchverbindung beinhalten, denen kein SIP mehr folgt und für die daher eine aseptische Durchführung essenziell ist. Hierbei geht es nicht nur um ...
-
Mischgranulatoren
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 131 (2017))
Mischgranulatoren / Produkte
Mit dem Mischgranulator MGT bietet Lödige *) ein System zum Mischen und Granulieren von pharmazeutischen Pulvern und Granulaten. In einem vertikalen, zylindrischen Mischbehälter rotiert mit geringem Abstand zu Behälterwand und -boden ein dreiflügeliges Mischwerkzeug. Dies führt zu kurzen Mischzeiten und hoher Mischgüte und ermöglicht einen gezielten Aufbau von Granulaten. Ein separat angetriebener Messerkopf dient zum Aufschließen evtl. vorhandener Agglomerate sowie zur gleichmäßigen Befeuchtung und Granulierung. Die Flüssigkeitszugabe erfolgt gravimetrisch oder direkt in den Wirkungsbereich des Messerkopfs, um eine bestmögliche Verteilung zu gewährleisten. Das optionale Feuchtsieb an der Entleerung erzeugt eine homogene Größenverteilung der Granulate. Die PC/SPS-basierte Steuerung ist mit ... -
Softwaregestützt kennzeichnen
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 72 (2017))
Softwaregestützt kennzeichnen / Chancen für die Produktion – auch vor dem Hintergrund der EU-Fälschungsschutzrichtlinie · Kürten-Kreibohm S · Bluhm Systeme GmbH, Rheinbreitbach
In der Pharmaindustrie werden nicht nur an die Produkte extrem hohe Anforderungen gestellt, sondern auch an die im Produktionsprozess eingesetzte Technik. Systeme und Anlagen müssen zuverlässig und stabil laufen. Gleichzeitig geht es darum, die Produktion zu optimieren, um wettbewerbsfähig zu bleiben. Da sich Kennzeichnungssysteme an neuralgischen Punkten in der Produktion befinden, könnten sie „nebenbei“ einen Mehrwert schaffen, wenn eine entsprechende Software zum Einsatz käme. Mithilfe von Software könnten die Kennzeichnungssysteme nicht nur sicher und zentral gesteuert werden. Würden die Geräte und Anlagen miteinander vernetzt und regelmäßig „befragt“, könnten auch Schwachstellen und Potenziale in der Produktion aufgezeigt werden. Der Beitrag legt ...
-
Spritzenlabel
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 129 (2017))
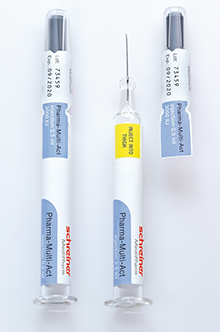
Spritzenlabel / Produkte
Schreiner MediPharm *) hat eine neuartige Kennzeichnungslösung für Spritzen entwickelt: Pharma-Multi-Act. Das Besondere: Eine ins Kennzeichnungslabel integrierte, mit einer Perforation versehene Lasche endet auf der Spritzenkappe. Öffnet man die Kappe, wird der Erstöffnungsschutz des Labels automatisch entlang der Perforation ausgelöst. Dadurch erfolgt die Öffnung des Etiketts und des Gefäßes gleichzeitig mit einer Handbewegung, ohne dass ein weiterer Schritt zur Entfernung des Siegels notwendig ist. Durch den Öffnungsprozess entsteht ein leicht zugängliches, abnehmbares Dokumentationsteil auf der Kappe, das selbst mit Handschuhen einfach abzulösen ist. Die Fläche unterhalb des abnehmbaren Teils kann zudem als Indikatorfeld für unterschiedlichste Funktionen genutzt werden. Dies ... -
GMP-Reinraumsysteme
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 128 (2017))
GMP-Reinraumsysteme / Produkte
Das GMP-Reinraumsystem CleanSteriCell® von SCHILLING ENGINEERING *) wurde für den Produkt- und Personenschutz in der Pharmaproduktion entwickelt. Die innovativen Reinräume und Reinraumlabore sind modular aufgebaut und können dank der silikonfreien GMP-Dicht-Clip-Verbindung flexibel erweitert und umgebaut werden. Eine Umluftführung innerhalb der Reinraumwände, die die bereits gekühlte und gefilterte Luft erneut in den Kreislauf führt, und der Einsatz von sehr wartungsarmen ULPA-U15-Hochleistungsfiltern sorgen für hohe Sicherheit bei reduziertem Energieverbrauch. Neu entwickelt wurden GMP-konforme LED-Lichtbänder innerhalb der Aluminiumprofile, die eine ausgewogene und sparsame Beleuchtung sicherstellen. Über das bedienerfreundliche Kontrollsystem CR_Control®, das über einen zentralen Touchscreen und auch per App mobil gesteuert werden ... -
Rundum-Etikettieranlage
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 131 (2017))
Rundum-Etikettieranlage / Produkte
Die kompakte Rundum-Etikettieranlage 152E von HERMA *) deckt ein breites Spektrum an Produktdimensionen ab, lässt sich jedoch z. B. von vornherein mit einer kompletten Pharma-Ausstattung versehen. Dazu gehören z. B. Module für den variablen Datendruck, für die Kontrolle von Aufdrucken und Codes bzw. für die Etikettenanwesenheit sowie für einen entsprechenden Auswurf. Die Version mit Etiketten-Anrollband kommt gänzlich ohne Formatsätze aus. Daraus resultieren nicht nur besonders kurze Rüstzeiten, sondern auch eine beachtliche Leistung von bis zu 100 Produkten pro Minute. Bei der Version mit Rollenprisma lässt sich eine höhere Präzision erzielen. In dieser Variante kommt die Anlage auf etwa 90 Produkte pro ... -
25 Jahre PAMAS
Rubrik: Spektrum
(Treffer aus TechnoPharm, Nr. 02, Seite 126 (2017))
25 Jahre PAMAS / Spektrum
Die PAMAS GmbH, führender Hersteller von Flüssigpartikelzählern, feiert in diesem Jahr ihr 25-jähriges Bestehen. Das inhabergeführte, mittelständische Unternehmen mit Sitz in Rutesheim entwickelt, fertigt und vertreibt laseroptische Partikelmessgeräte für Flüssigkeiten aller Art. Partikelmessgeräte haben sich in den vergangenen 25 Jahren zu einem unverzichtbaren Werkzeug für die Reinheitskontrolle entwickelt. Nach seinem Chemiestudium war Geschäftsführer und Firmengründer Gerhard Schreck über ein Jahrzehnt auf dem Gebiet der Partikelmesstechnik tätig gewesen, bevor er die PAMAS GmbH am 1. Juni 1992 gründete. Das erste Modell für pharmazeutische Anwendungen, das die PAMAS GmbH zur Serienreife entwickelte, war das Modell PAMAS SVSS (Small Volume Syringe System). Damit ... -
HPAPI-Handlings- und Verpackungsanlagen
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 94 (2017))
HPAPI-Handlings- und Verpackungsanlagen / Anforderungen an Personenschutz und GMP · Glättli M · SKAN AG, Allschwil (Schweiz)
Um im Anlagenbau von pharmazeutischen Produktionsanlagen den Spagat zwischen Health, Safety and Environment (HSE) und Good Manufacturing Practice (GMP) zu meistern, ist ein Umdenken in Richtung integriertes Anlagendesign notwendig. Dies erfordert passende Lösungen vor allem im Bereich der Schnittstellen zu einem Prozess, welcher innerhalb eines Containment-Bereichs ablaufen soll – besonders bei Highly Potent Active Pharmaceutical Ingredients (HPAPIs). Die Bestrebungen gehen in Richtung einer Standardisierung solcher Schnittstellen, was ein schnelleres Anlagendesign ermöglichen soll.
-
Resthärtemessgerät
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 130 (2017))
Resthärtemessgerät / Produkte
BWT Pharma & Biotech *) führt das Resthärtemessgerät AQU@Sense auf dem Markt ein. Durch den Verzicht auf Reagenzien ist es eine einfache und wartungsarme Alternative zu anderen auf Titration basierenden Resthärtemesssystemen. Im einfachen Betriebsmodus misst das Gerät zyklisch die Resthärte und schaltet bei Überschreitung eines einstellbaren Grenzwerts einen potenzialfreien Kontakt. Im erweiterten Betriebsmodus werden 2 Messstellen überwacht. Mit der Automatisierung ist die qualitätsgesteuerte Regeneration von 2 Enthärtersäulen möglich: Der AQU@Sense erfasst die Erschöpfung des Arbeitsfilters und schaltet für die externe Steuerung einen Kontakt. Diese wechselt die Enthärtersäule samt Messpunkt und startet die Regeneration. Diese kapazitätsgesteuerte Regeneration ist so sicher ... -
Lebenszyklus-Risikoanalyse in der Qualifizierung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 114 (2017))
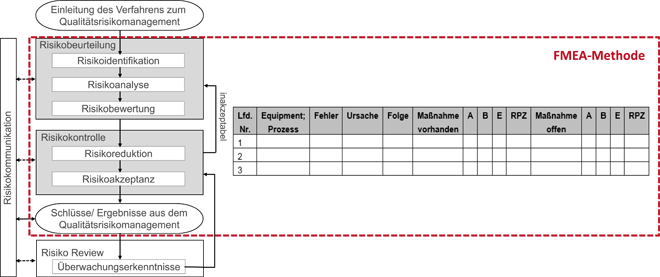
Lebenszyklus-Risikoanalyse in der Qualifizierung / Implementierung eines software-unterstützten Life-Cycle-Risikomanagement-Prozesses – Teil 2 * Teil 1 dieses Beitrags ist erschienen in TechnoPharm 7, Nr. 1, (24–30) (2017). · Gübitz B, Feil U · VTU Engineering GmbH, Raaba-Grambach (Österreich) und Biotest AG, Dreieich
Im ersten Teil dieses Beitrags wurden die Anforderungen an ein GMP-konformes Risikomanagement sowie die ersten Schritte eines Life-Cycle-Risikomanagements für die Qualifizierung beschrieben – nämlich die risikobasierte Definition des Qualifizierungsumfangs (Impact Assessment) sowie die Sicherstellung der Traceability zwischen Betreiberanforderung und Ausschreibungsunterlagen im Projekt. Um die Qualifizierungstiefe der im Impact Assessment als GMP- und damit als qualifizierungsrelevant eingestuften Anlagen festzulegen, werden im Projekt rund 40 Risikoanalysen für Prozessanlagen und Prozessnebenanlagen (Aqua Purificata (AP-Wasser), raumlufttechnische Anlagen, etc.) und 30 Risikoanalysen für Laborgeräte durchgeführt. Diese technischen Risikobetrachtungen werden im Projekt nach der Spezifikations- und Ausschreibungsphase (URS, LH) und vor der DQ-Phase erstellt (Abb. 2). Sie ...
Sie sehen Artikel 10211 bis 10220 von insgesamt 11116
- Erste Seite
- 1020
- 1021
- 1022
- 1023
- 1024
- Letzte Seite