Case Study Blow-Fill-Seal | Beitrag aus Tech4Pharma 16 | Nr. 2 | Seite 62-67 (2026)
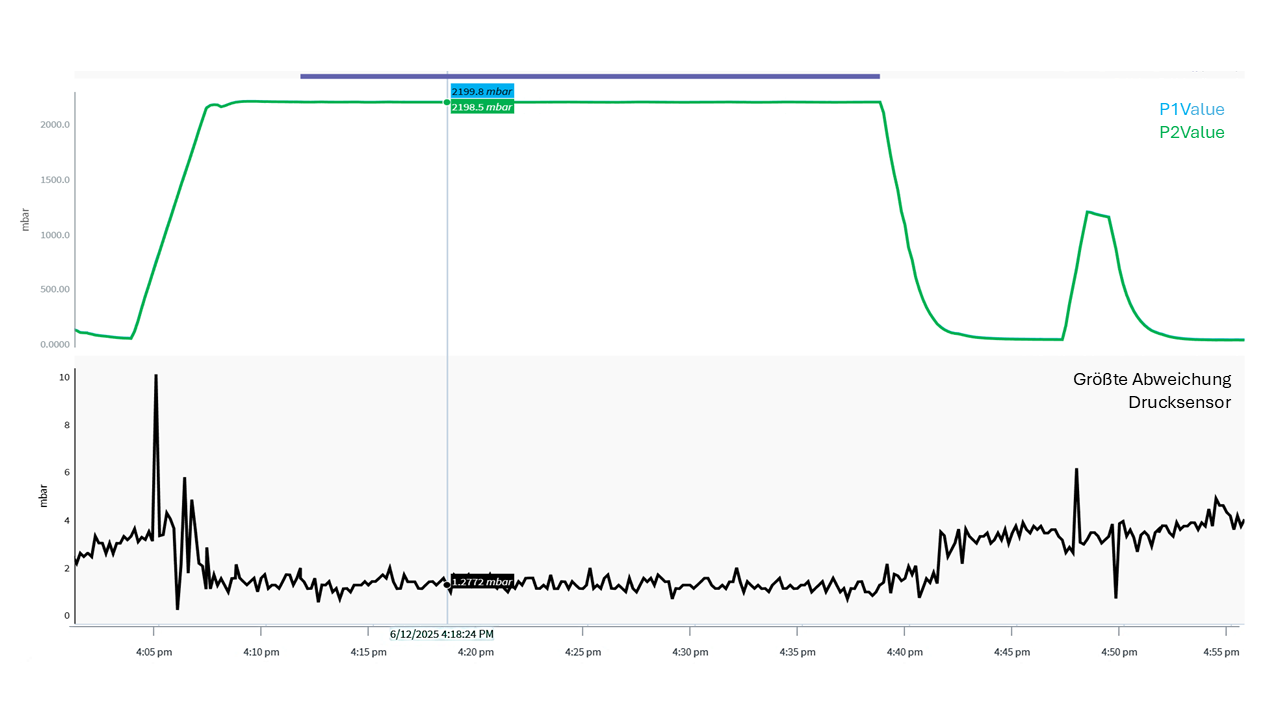
28.05.2026This application report covers the development and initial installation of modular systems for integrity testing and optical inspection of freshly filled blow-fill-seal containers at Pioneer Co. for ...
SENSOR+TEST 2026: Sensorik, Messtechnik und Industrial AI verschmelzen zu intelligenten Systemen
03.06.2026Nürnberg wird vom 9. bis 11. Juni 2026 erneut zum internationalen Treffpunkt für Sensorik, Mess- und Prüftechnik. Die SENSOR+TEST erwartet rund 5.000 Fachbesucher sowie rund 320 Aussteller aus ...
Kühlfahrzeuge für Pharmatransporte
05.06.2026Für den Transport sensibler pharmazeutischer Produkte gelten besonders hohe Anforderungen an Temperaturführung, Dokumentation, Qualität und Sicherheit. Kiesling bietet GDP-qualifizierte Lösungen ...
BD Rowa führt vorausschauendes Wartungskonzept ein: Echtzeitdaten und KI ersetzen feste Serviceintervalle
03.06.2026BD Rowa führt ein neues vorausschauendes Wartungskonzept für Automatisierungssysteme in Apotheken ein. Künftig bestimmen Echtzeit-Maschinendaten, intelligente Algorithmen und CRM-gestützte ...
Zukunftssicherheit mit KHS-Umbaukatalog
05.06.2026195 technische Standardlösungen bietet die KHS Gruppe in ihrem interaktiven Umbaukatalog an. Diese ermöglichen es, die Lebensdauer von Bestandsmaschinen signifikant zu verlängern, Ressourcen zu ...
Carlos Negro übernimmt Vorsitz des World Chemical Engineering Council
03.06.2026Der Weltrat für Chemieingenieurwesen (World Chemical Engineering Council, WCEC) hat einen bedeutenden Führungswechsel bekannt gegeben: Professor Carlos Negro (Spanien) hat das Amt des Vorsitzenden ...
meistgelesen

Beitrag aus der Ausgabe 1/2026 der Zeitschrift Tech4Pharma
Neue Lösung zum Konditionieren hochtoxischer APIs unter Reinraumbedingungen
Content Marketing
Biopharmazeutische Active Pharmaceutical Ingredients (APIs) sind hochpotent. Ihre Herstellung erfordert einen besonderen Schutz der Mitarbeiter und häufig eine Klimakonditionierung des Produkts. Weiss Pharmatechnik hat dafür einen Isolator mit einem Klimaschrank als geschlossenes System zu einem Reinraum kombiniert.APIs bieten zahlreiche innovative Möglichkeiten zur Behandlung komplexer Krankheiten wie Epilepsie, Depressionen und Alzheimer. Sie ...
Beitrag aus der Ausgabe 4/2025 der Zeitschrift Tech4Pharma
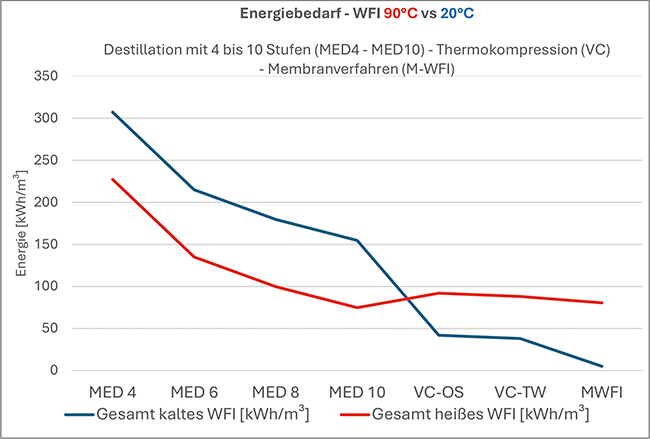
Serie: Energetische Analyse von WFI-Systemen
Teil 2*Teil 1 dieser Serie s. Tech4Pharma 2025;15(3):158–163.: WFI-Erzeugung – Auswahlkriterien und Energiebilanz
Der erste Serienteil bot einen Überblick über die gängigen Verfahren zur Herstellung von Wasser für Injektionszwecke (WFI): Mehrstufendestillation, Thermokompression und membranbasierte Systeme. Die Funktionsweise, Betriebsmöglichkeiten und energetischen Eigenschaften der Technologien wurden systematisch dargestellt. Ein besonderer Fokus lag auf Nachhaltigkeitsaspekten und integrierten Energiesparmaßnahmen.Im dritten Serienteil werden die ...
Beitrag aus der Ausgabe 2/2026 der Zeitschrift Tech4Pharma
Fülltechnologie für flüssige, sterile Formen
Rüsten – Betreiben – Füllsystemtypen und deren Eigenschaften – Teil 1
Das aseptische Befüllen von Packmitteln mit sterilen Flüssigkeiten ist ein Kernprozess bei der Herstellung parenteral zu verabreichender Medikamente. Dabei kommt dem Füllprozess die Aufgabe zu, das Medikament homogen in seiner Zusammensetzung, präzise in seiner Menge, unverändert in seinem pharmakologischen Wirkprofil und kontaminationsfrei in das sterile Packmittel zu dosieren, aus dem später die Dosen für die Patienten entnommen ...
Top Themen
Beitrag aus der Ausgabe 2/2026 der Zeitschrift Tech4Pharma
Einstieg in Continuous Manufacturing
Technologische, prozessuale und entwicklungsrelevante Aspekte der kontinuierlichen Feuchtgranulation
In der Pharmaindustrie werden Granulationsprozesse zunehmend unter den Aspekten der Effizienzsteigerung und Kostenoptimierung betrachtet. Ziel der Feuchtgranulation ist es, aus feinem Pulver gröbere Agglomerate zu erzeugen. Agglomerate können aus festen und trockenen Körnern bestehen, wobei jedes Korn ein Agglomerat aus Pulverpartikeln mit genügend Festigkeit darstellt. Granulate können direkt als Arzneimittel verwendet werden oder dienen als ...

Vorschau (Änderungen vorbehalten)
Beitrag aus der nächsten Ausgabe 3/2026 der Zeitschrift Tech4Pharma
(erscheint am 09.09.2026)
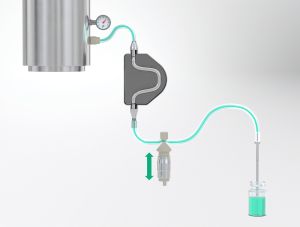
Fülltechnologie für flüssige, sterile Formen / Rüsten – Betreiben – Füllsystemtypen und deren Eigenschaften – Teil 2
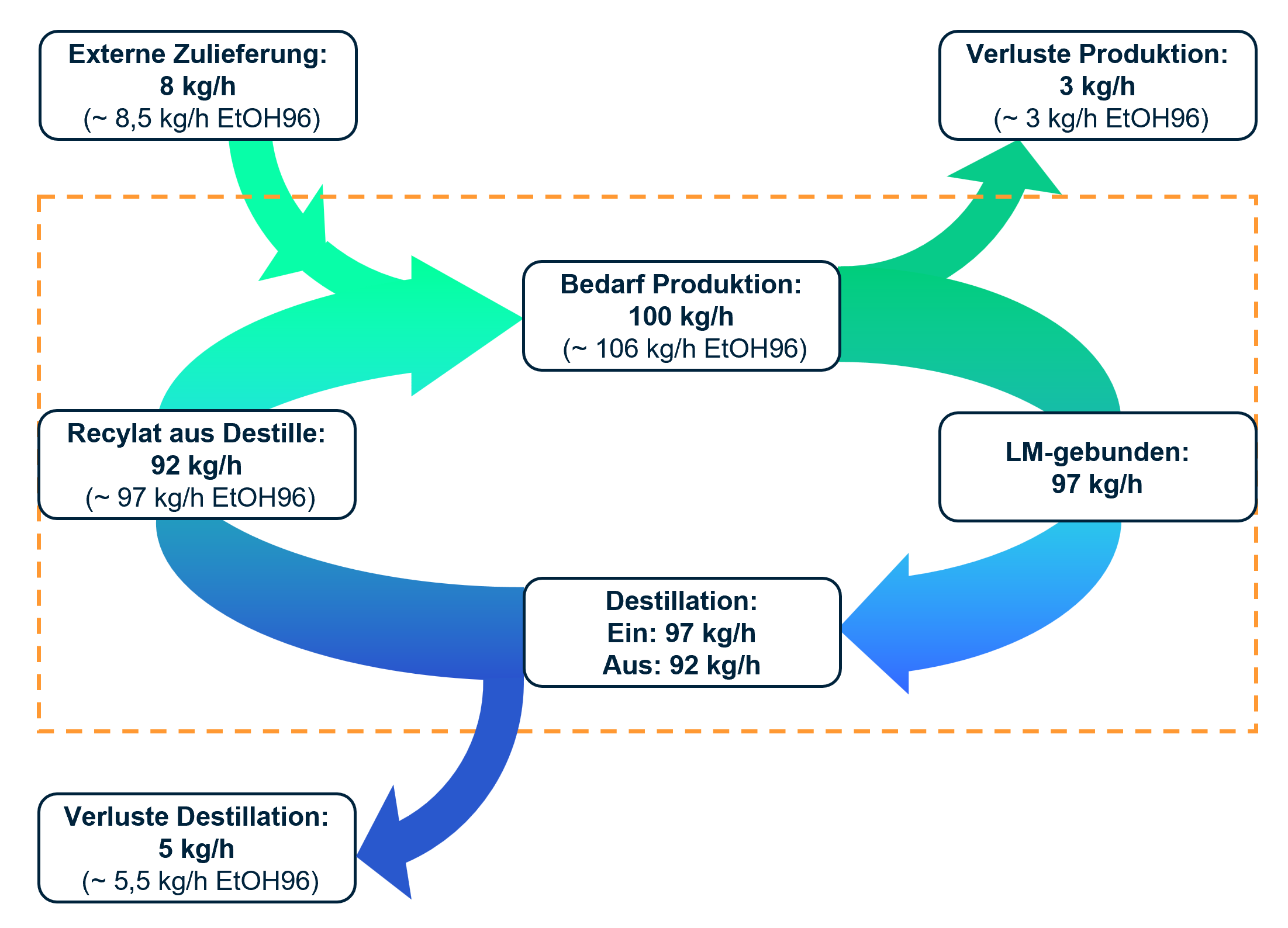
Im ersten Teil dieses Fachbeitrags wurden die regulatorischen Vorgaben für das Abfüllen flüssiger Pharmazeutika sowie das aseptische Rüsten gemäß des EU-GMP Annex 1 erläutert. Weiterhin wurden die Grundlagen des Füllprozesses und das Strömungsverhalten von Fluiden beschrieben. Dieser zweite Teil behandelt den Aufbau und die Funktionsweise gängiger Fülltechnologien. Zusätzlich werden Möglichkeiten zur Reduktion von Produktverlust vor, während und nach der Produktion aufgezeigt. Abschließend werden Anforderungen verschiedener Produktklassen von Medikamenten erläutert sowie die damit einhergehende Wahl eines geeigneten Füllsystems begründet.