Integrierte Herstellplattformen
Industrialisierung der Produktion von autologen Zell- und Gentherapien
Biotechnologie
Zusammenfassung
Autologe Zell- und Gentherapien haben in den letzten Jahren bahnbrechende Erfolge in der Behandlung bereits austherapierter Patienten erzielt. Hierbei ist die kommerzielle Herstellung dieser autologen Zell- und Gentherapien aufgrund des zugrunde liegenden Paradigmas „Ein Prozess – Ein Produkt“ eine äußerst komplexe Herausforderung in der Bioprozesstechnik.
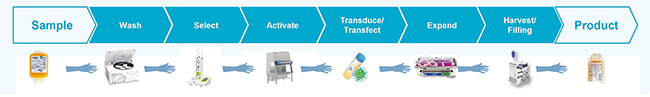
Eine Möglichkeit, diesen Herausforderungen zu begegnen, ist die Verwendung von flexibler und gleichzeitig industrialisierungsreifer Plattformtechnologie, der es gelingt, sich ständig wechselnden Anforderungen mit ausreichender Robustheit anzupassen. Dieser Fachbeitrag wird für den aktuell am weitesten kommerziell verbreiteten Typen von autologen Zell- und Gentherapien, den Chimeric Antigen Receptor T-Cells (CAR-T), einen fiktiven Produktionsablauf auf einer vollintegrierten Herstellplattform inkl. Schnittstellen zu anderen Aspekten der vollumfänglichen Lieferkette (z. B. adäquate Qualitätskontroll-Systeme) aufzeigen.
Korrespondenz:
Dr. Silvio Weber
Miltenyi Biotec B.V. & Co. KG, Friedrich-Ebert-Str. 68,
51429 Bergisch Gladbach
silviow@miltenyibiotec.de
 | Dr. Silvio Weber ist aktuell Senior Manager Product-Market-Fit Immunotherapy und verantwortet in dieser Funktion den Bereich der industriellen Prozessentwicklung bei Miltenyi Biotec. Er hat mehr als 15 Jahre Erfahrung in der angewandten Forschung und Entwicklung und hat in dieser Zeit eine große Bandbreite an Projekten zur industriellen Prozessentwicklung von ATMPs geleitet. Er hat sein Diplom der Biochemie von der Universität Bielefeld und seinen Doktor der Biochemie von der Universität Kiel |
Schließen Sie hier ein Abonnement ab und profitieren Sie von den vielseitigen Nutzungsmöglichkeiten.