Innovationen im pharmazeutischen Reinraum | Beitrag aus cleanroom & processes 5 | Nr. 2 | 68-73 (2026)
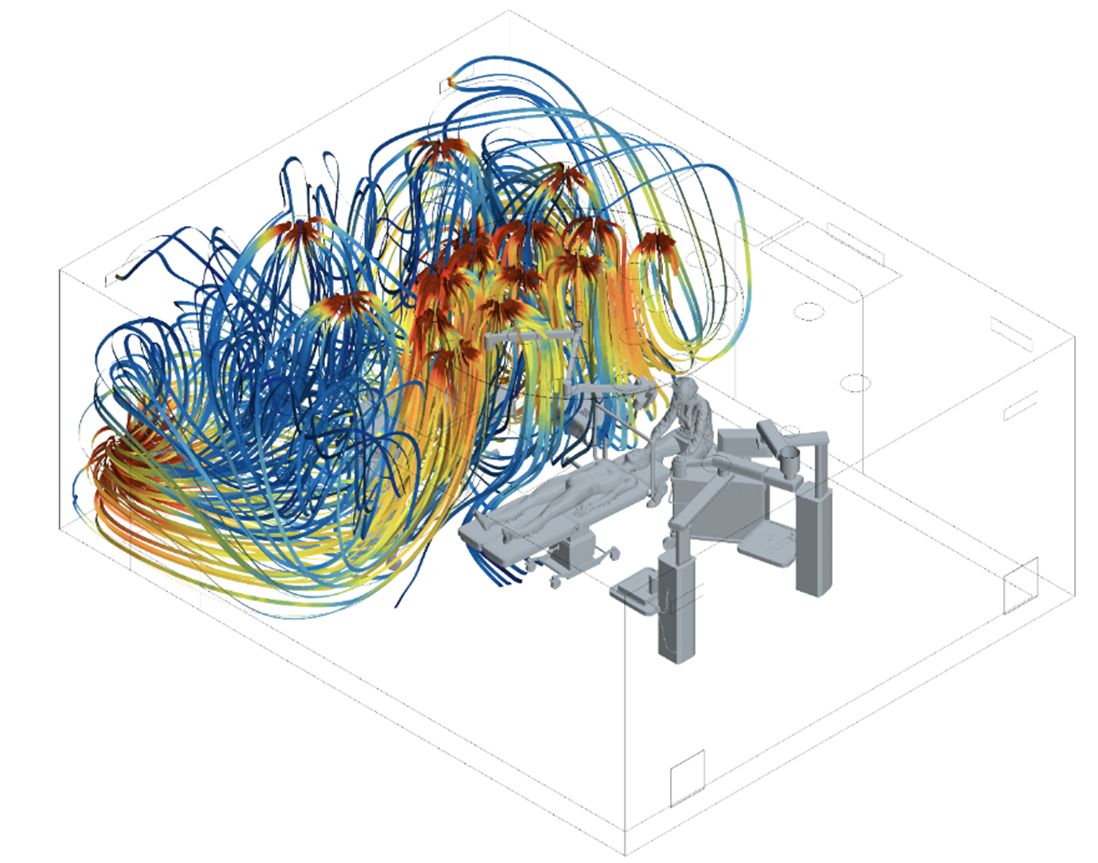
01.06.2026Reinräume in der pharmazeutischen Produktion stellen höchste Anforderungen an Hygiene, Produktqualität und Prozesssicherheit. Klassische Verfahren stoßen dabei oft an Grenzen – z. B. wenn ...
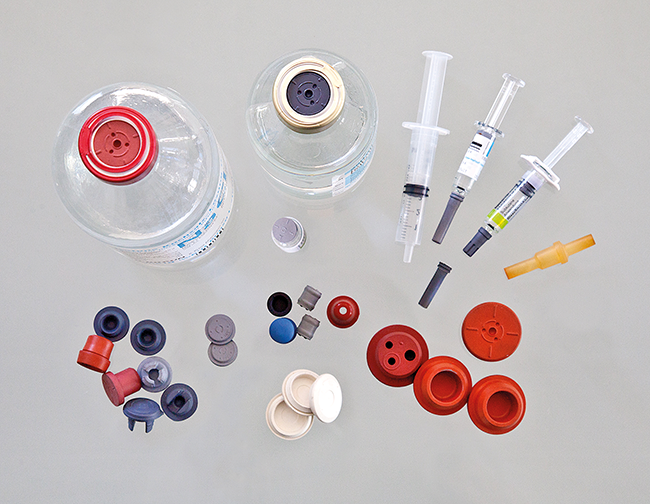
Aseptische Verarbeitung von RTU Spritzen, Vials und Karpulen im Nest
03.06.2026Der Einsatz von ready-to-use Packmitteln (RTU) in der pharmazeutischen Industrie steigt seit vielen Jahren stetig an. Dafür gibt es mehrere Gründe: zunehmend kleiner werdende Batch-Größen, ...
Prüfung von Reinräumen, Reinraumanlagen und Reinraumkomponenten
03.06.2026Prüfgrundlage sind die relevanten Teile von DIN EN ISO 14644ff und Richtlinien VDI 2083ff sowie die EU-Richtlinie 2003/94/EG mit zugehörigen GMP-Leitlinien.
Reinraumklassen nach ISO 14644-1 und GMP – einfach erklärt
29.05.2026Als Reinraum bezeichnet man jeden Raum, in dem Maßnahmen getroffen werden, um Produkte, Prozesse oder Anwendungen vor Verunreinigungen zu schützen. Doch nicht jeder Reinraum ist gleich sauber – ...
Warum werden für Reinräume spezielle Ausstattungen benötigt?
28.05.2026Reinräume sind darauf ausgelegt, Kontaminationen zu minimieren. Reinräume der Klasse ISO-5 zum Beispiel weisen maximal 3.520 Schwebepartikel mit einer Größe von 0,5 µm oder mehr pro Kubikmeter ...
meistgelesen
Beitrag aus der Ausgabe 2/2026 der Zeitschrift cleanroom & processes
Schnee statt hochreinem Wasser
Medizin- und Pharmaprodukte sicher und ressourcenschonend reinigen
Das Spektrum an medizintechnischen Produkten und pharmazeutischen Erzeugnissen, die verpackt werden müssen, ist enorm vielfältig und stellt besondere Anforderungen an die Reinigung während der Herstellung. Dabei ist ein produktspezifisch definiertes Reinheitslevel zuverlässig zu erfüllen. Hinzu kommen regulatorische Vorgaben, die eingehalten werden müssen. Entsprechend ist ein Reinigungsprozess dann für die Herstellung von Medizintechnik- und ...
Beitrag aus der Ausgabe 4/2025 der Zeitschrift cleanroom & processes
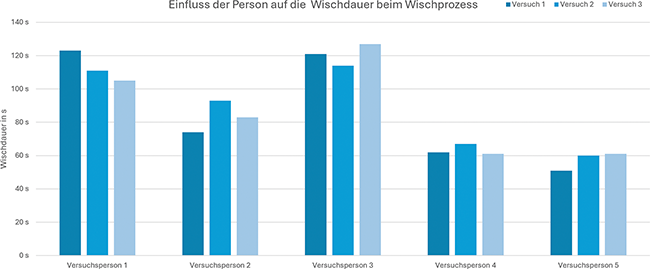
Reinigungseffizienz und Qualitätskonstanz
Entwicklung und Einsatz eines intelligenten Wischmopphalters für optimierte Reinraum-Wischprozesse
Reinräume und die betriebliche Umsetzung der Kontaminationskontrolle in diesen Räumen sind grundlegende Voraussetzungen für Branchen mit hohen Anforderungen an Hygiene und Sauberkeit wie in der Pharmazie, Medizintechnik, Biotechnologie, Mikroelektronik oder in der Lebensmittelindustrie. Durch die Coronakrise stiegen die Anforderungen insbesondere in der Pharmazie und im Gesundheitswesen nochmals an. In der Pharmaindustrie wurden zudem die ...
Beitrag aus der Ausgabe 2/2025 der Zeitschrift cleanroom & processes
Hydraulikpressen
Innovative Prozess- und Anlagentechnik für Reinraumanwendungen
Bei der Fertigung von Elastomerprodukten im Reinraum werden an Hydraulikpressen eine Reihe von Anforderungen hinsichtlich Präzision, Temperaturhomogenität, Normenkonformität und Prozessüberwachung gestellt. Für die Reinraumtauglichkeit der Anlagen sind u. a. die ISO 14644-14 [1] bzw. VDI 2083 Blatt 9.1 [2] relevant. Eine geringe Partikellast wird v. a. durch eine umfassende Automation der ...
Top Themen
Beitrag aus der Ausgabe 2/2026 der Zeitschrift cleanroom & processes
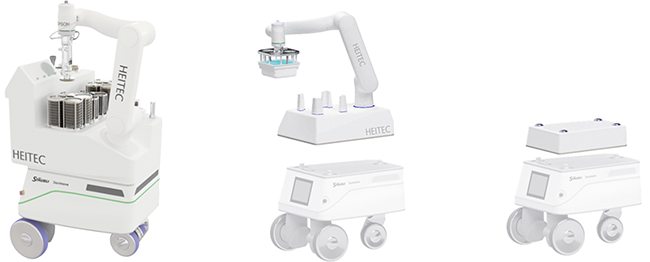
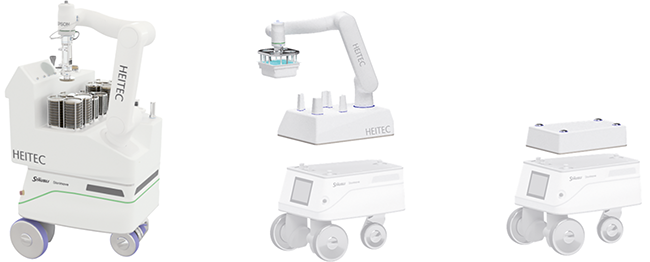
Innovationen im pharmazeutischen Reinraum
Kontaktlose Authentifizierung, mobile Robotik und intelligente Bedienkonzepte für die Pharmaproduktion
In hochreinen Produktionsbereichen der Pharmaindustrie steht die Vermeidung von Kontaminationen an oberster Stelle. Das größte Risiko geht dabei vom Menschen aus, weshalb Reinräume nur von autorisiertem Fachpersonal betreten werden dürfen. Gleichzeitig erfordern moderne Herstellprozesse eine lückenlose Kontrolle und Dokumentation, um Qualität und Compliance – etwa mit den GMP-Regularien – sicherzustellen. Traditionelle Verfahren ...

Vorschau (Änderungen vorbehalten)

Beitrag aus der nächsten Ausgabe 03/2026 der Zeitschrift cleanroom & processes
(erscheint am 18.09.2026)
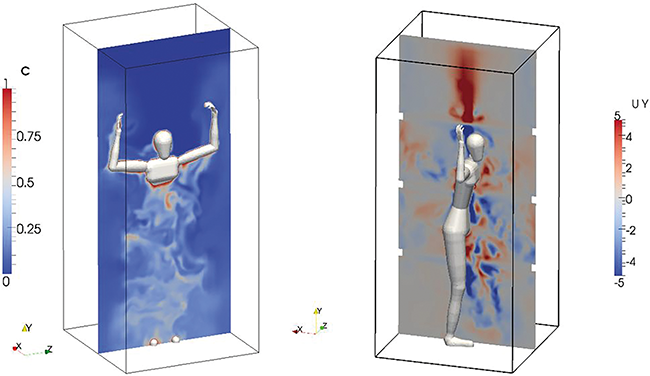
Trockenraum und Mensch - Wechselwirkungen und Beeinflussung
Die Produktion von Batteriezellen erfordert Rein- und Trockenräume mit hoher Partikelreinheit und extrem niedriger Luftfeuchte. Während die Technik solcher Umgebungen gut beschrieben ist, ist der Einfluss des Personals auf den Taupunkt sowie die Rückwirkung des trockenen Klimas auf die Mitarbeitenden kaum untersucht. Im Rein- und Trockenraumlabor des Fraunhofer IPA wurden Versuche zur durch Personen verursachten Veränderung des Taupunkts durchgeführt. Auf Basis der Ergebnisse wurden Verhaltensregeln sowie organisatorische und technische Maßnahmen abgeleitet, die sowohl die Stabilität des Trockenraumklimas als auch den Gesundheitsschutz unterstützen.