Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Haidacher R.
In der Rubrik Zeitschriften haben wir 1 Beitrag für Sie gefunden
-
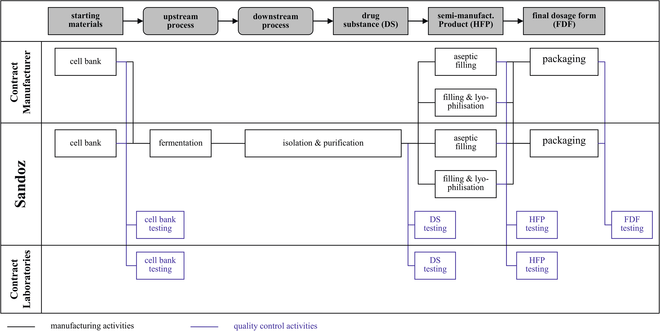
Das neue Site Master File
Rubrik: IT
(Treffer aus TechnoPharm, Nr. 05, Seite 283 (2014))
Das neue Site Master File / Beispiel einer praktischen Umsetzung · Haidacher R, Simon V · Sandoz GmbH, Kundl (Österreich) und Simon Pharma Consult e.U., Garsten (Österreich)
Anfang 2011 wurden von der Europäischen Kommission und der Pharmaceutical Inspection Convention / Pharmaceutical Inspection Cooperation Scheme (PIC/S) die endgültigen Dokumente zum Site Master File (SMF) „ Explanatory Notes on the Preparation of a Site Master File“ veröffentlicht [ 1 , 2 ]. Seitdem besteht die Verpflichtung die SMFs gemäß dieser regulatorischen Grundlage (nachfolgend kurz als „ Explanatory Notes“ bezeichnet), die in die EU Guideline Part III [ 3 ] integriert wurden, zu verfassen. Folglich bestand diese Aufgabenstellung auch für den Geschäftsbereich Biopharmaceuticals der Sandoz GmbH am Standort Kundl . Die Erstellung des SMF soll in diesem Beitrag ...