Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Otterbach S.
In der Rubrik Zeitschriften haben wir 2 Beiträge für Sie gefunden
-
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 01, Seite 16 (2020))
Wagner B | Brinz T | Otterbach S
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung / Teil 2*Teil 1 dieses Beitrags ist erschienen in TechnoPharm 9, Nr. 5, 278–285 (2019). · Wagner B, Brinz T, Otterbach S · Bosch Packaging Technology GmbH, Waiblingen
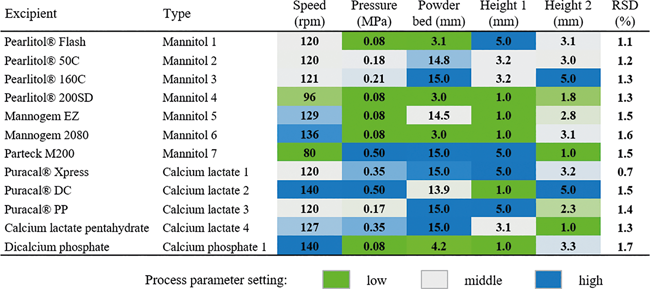
Im ersten Teil dieses Beitrags wurde die Methode der automatisierten Inbetriebnahme (Automated Process Development, APD) vorgestellt. Die automatisierte Inbetriebnahme verwendet statistisch optimierte Versuchspläne und führt diese automatisch, schnell und bei verringertem Pulververbrauch auf dem entsprechenden System oder Anlage durch. Durch die Verwendung der statistischen Versuchsplanung (DoE) sinkt die Anzahl der Versuche gegenüber der klassischen Versuchsplanung. Des Weiteren reduziert sich durch die Automation bzw. die automatisierte Durchführung der Versuche der Aufwand, der notwendig ist, um die Prozessparameter an der Maschine einzustellen. Die kritischen Qualitätsmerkmale (CQA) werden am Ende direkt online oder inline bei der Durchführung der Versuche erfasst. Für die Entwicklung ...
-
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 278 (2019))
Wagner B | Brinz T | Otterbach S
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung / Teil 1 · Wagner B, Brinz T, Otterbach S · Bosch Packaging Technology GmbH, Waiblingen
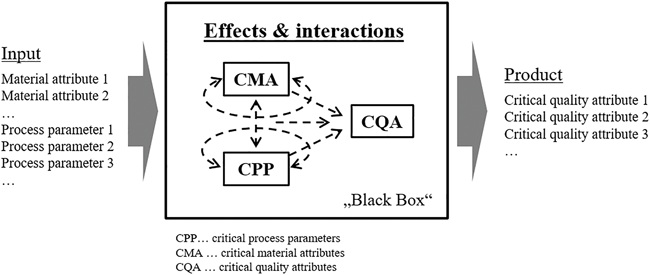
Quality by Design (QbD) Capsule Filling Process Development Design of Experiment (DoE) Powder Filling Ein detailliertes Prozessverständnis ist für die Validierung eines Prozesses unumgänglich. Mit dem Begriff Quality by Design (QbD) setzte die U.S. Food and Drug Administration (FDA) ein Paradigma für die pharmazeutische Prozessentwicklung [1]. Bekannt aus anderen Industrien (etwa Automobil) beschreibt QbD die Idee, dass Qualität nicht erst nachträglich im Produkt getestet wird, sondern bereits bei der Planung und Entwicklung eines Prozesses entsteht. Voraussetzung: Alle entscheidenden Einflüsse auf das Arzneimittel und den Produktionsprozess sowie deren Wechselwirkungen untereinander sind bekannt, und diese können auch gesteuert oder kontrolliert werden. Dann ...