Technologie zur schnellen Identifizierung unbekannter Moleküle in großem Maßstab
26.04.2024Start-up Isospec Analytics sammelt 1,9 Millionen Dollar ein...
CureVac ernennt Thaminda Ramanayake zum neuen CBO
26.04.2024CureVac N.V. gab am 24.04.2024 bekannt, dass Thaminda Ramanayake zum Chief Business Officer (CBO) ernannt wurde. Die Ernennung wird zum 1. Juni 2024 wirksam.

Kooperation von Testo und Liebherr ermöglicht breitere Nutzung von Vernetzungslösung
25.04.2024In Medizin, Forschung und Laboren haben Präzision und Sicherheit oberste Priorität – auch bei der Lagerung empfindlicher Substanzen. Die speziell für diese...
Schlaganfälle: Akutbehandlung top, Nachsorge teilweise ein Flop
25.04.2024Ein Schlaganfall verändert alles: Das Leben der Betroffenen und ihrer Angehörigen. Zwar ist es in der Vergangenheit gelungen, die Sterblichkeit nach einem Hirninfarkt zu reduzieren. Aber bei der ...
Top Downloads

Beitrag aus der Ausgabe 10/2023 der Zeitschrift pharmind
Bayer
pharmind • In Wort und Bild
Der Aufsichtsrat der Bayer AG hat Heike Prinz mit Wirkung zum 1. Sept. 2023 als Chief Talent Officer und Arbeitsdirektorin in den Vorstand des Unternehmens berufen. Zuvor hatten sich Sarena Lin und der Aufsichtsrat einvernehmlich darauf geeinigt, Lins Vertrag als Mitglied des Vorstands nicht über den 31. Jan. 2024 hinaus zu verlängern.Prinz blickt auf eine fast 37-jährige Karriere bei Bayer zurück. Derzeit ist sie als ...
Beitrag aus der Ausgabe 10/2023 der Zeitschrift pharmind
KI in der Medizin – Produkthaftung
pharmind • Buchbesprechungen
Der Einsatz von Künstlicher Intelligenz (KI) in der Medizin revolutioniert das Gesundheitswesen, wirft jedoch auch neue Haftungsfragen auf. Die Autorin untersucht, ob das europäische Produkthaftungsrecht auf KI-basierte Medizinprodukte anwendbar ist und einen angemessenen Risikoausgleich zwischen Herstellern und Nutzern schaffen kann.Dazu werden alle Haftungsvoraussetzungen analysiert und ein Maßstab zur Bewertung der Fehlerhaftigkeit ...

Beitrag aus der Ausgabe 10/2023 der Zeitschrift pharmind
Rentschler Biopharma
pharmind • In Wort und Bild
Rentschler Biopharma SE gab bekannt, dass das Unternehmen Benedikt von Braunmühl zum Chief Executive Officer (CEO) berufen hat. Benedikt von Braunmühl verfügt über fast 30 Jahre Erfahrung im internationalen Gesundheitswesen und kann auf eine beeindruckende Erfolgsbilanz beim Umsetzen betrieblicher Strategien zur Erreichung unternehmerischer Wachstumsziele verweisen. Er trat seine Position am 19. Sept. 2023 an.Vor seinem ...
Branchenposter
Top Themen
Beitrag aus der Ausgabe 3/2024 der Zeitschrift pharmind
GMP-Plant für Entwicklung und Herstellung klinischer Prüfpräparate
Multifunktionales Gebäude bei Merck in Darmstadt
Das Wissenschafts- und Technologieunternehmen Merck erneuert sein Konzept und seine Herstell-Plant für klinische Prüfmuster. Das global agierende Familienunternehmen, gegründet 1668, setzt in allen Bereichen seiner 3 Business-Sektoren Healthcare, Life Science und Electronics auf den wissenschaftlichen Fortschritt zum Wohl von Patienten und seiner mehr als 64 000 Mitarbeiter. Mit seiner neuen GMP-Pilot-Plant, dem Technical ...

Beitrag aus der Ausgabe 1/2024 der Zeitschrift TechnoPharm
No-Touch Transfer (NTT)
Eine schlanke Lösung zur Einbringung vorsterilisierter Primärpackmittel in den Klasse-A-Bereich
In der pharmazeutischen Industrie hat das Interesse an der Verwendung vorsterilisierter Primärverpackungen bei der aseptischen Abfüllung von sterilen Arzneimitteln stark zugenommen [1, 2]. Auch die Lohnabfüller müssen flexibel reagieren und den Anforderungen der Abfüllung kleiner bis mittlerer Chargen gerecht werden, sodass sich vorsterilisierte Vials und Spritzen als neuer Industriestandard etabliert haben [3].In diesem Zusammenhang wurde das ...

Beitrag aus der Ausgabe 1/2024 der Zeitschrift cleanroom & processes
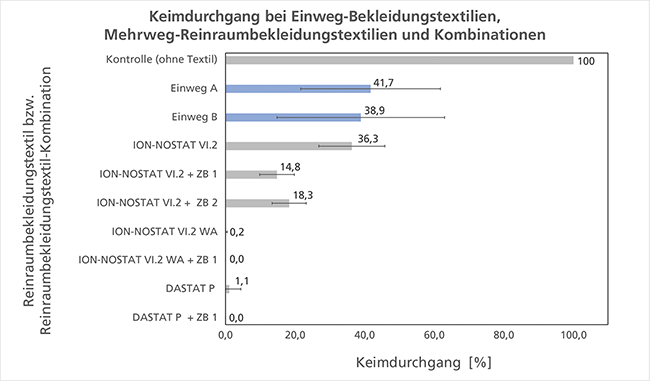
Bewährungsprobe für Reinraumbekleidung
Die ReBa2-Prüfmethode zur Bestimmung des Keimdurchgangs – Teil 2*Teil 1 dieses Beitrags s. cleanroom & processes 2023;2(4): 174–178.
Die quadratischen Messproben werden zugeschnitten, die Außen- bzw. Innenseite markiert und sterilisiert. Das Sterilisationsverfahren wird vorzugsweise entsprechend der geplanten Anwendung ausgewählt, z. B. Dampfsterilisation.Bei Materialien, die bereits in sterilem Zustand geliefert werden, ist eine aseptische Messprobenentnahme möglich.Die Komponenten Baumwollgewebe, Keimträger- sowie Abdeckfolie werden dampfsterilisiert.Das Prüfgerät ...

Vorschau (Änderungen vorbehalten)
Beitrag aus der nächsten Ausgabe 5/2024 der Zeitschrift pharmind
(erscheint am 31.05.2024)
Medizinisches Cannabis: Anforderungen an Verdampfer zu dessen Verabreichung – Teil 1
Die Verabreichung von medizinischem Cannabis erfolgt häufig mittels Verdampfung; das gilt insbesondere für Blüten, aber auch für zur Verdampfung geeignete Zubereitungen, wie Extrakte. Mit der im Mai 2021 in Kraft getretenen EU-Verordnung zu Medizinprodukten („Medical Device Regulation“, MDR) liegen nun detaillierte Vorgaben für Medizinprodukte vor, die zur Verabreichung von Arzneimitteln verwendet werden; das gilt auch für die Geräte, die zur Verdampfung von medizinischem Cannabis eingesetzt werden.

.png)
Beitrag aus der nächsten Ausgabe 2/2024 der Zeitschrift Tech4Pharma
(erscheint am 31.05.2024)
High-pressure cleaning in pharmaceutical production – A hitherto unjustly neglected technology! / Advantages and huge potential of sustainability and savings
High-pressure cleaning in pharmaceutical manufacturing can play a decisive role in current Good Manufacturing Practice (cGMP) cleaning automation with regards to sustainability and shorten downtimes for equipment facility installations. Significant reduction in media consumption and energy is possible compared to standard and manual cleaning methods. This article gives an overview about the methodology of high-pressure cleaning within pharmaceutical manufacturing processes, its advantages in general and on basis of a case study.

Beitrag aus der nächsten Ausgabe 02/2024 der Zeitschrift cleanroom & processes
(erscheint am 31.05.2024)
Realisierung von Gefriertrocknungsanlagen / Aktuelle regulatorische Anforderungen an Reinraumtechnologien zur aseptischen Prozessführung – Teil 1
Der Prozess der Gefriertrocknung, auch Lyophilisation genannt, nimmt in pharmazeutischen Herstellungsprozessen eine tragende Rolle bei der Stabilität von sensitiven Arzneimitteln ein. Für die Umsetzung der regulatorischen Anforderungen ist im Zusammenhang mit der Gefriertrocknung von sterilen Arzneimitteln insbesondere der Annex 1 zum Leitfaden der EU zur Good Manufacturing Practice (GMP) in der Fassung vom 25. Aug. 2022 zu berücksichtigen. Dieser Beitrag beschreibt die Anforderungen des Annex 1 an die gebotenen Reinraumtechnologien im Kontext mit Gefriertrocknungsanlagen. Darüber hinaus wird aufgezeigt, worauf geachtet werden muss, um Gefriertrocknungsprozesse entsprechend den GMP-Vorgaben in aseptischen Umgebungen durchführen zu können.