Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Müller I.
In der Rubrik Zeitschriften haben wir 14 Beiträge für Sie gefunden
-
Optimierung eines Coatingprozesses auf der Basis von Quality by Design
Rubrik: Originale
(Treffer aus pharmind, Nr. 08, Seite 1292 (2014))
Optimierung eines Coatingprozesses auf der Basis von Quality by Design / Stärk et al. • Coatingprozess-Optimierung · Stärk D, Weber E, Müller I · Hochschule Albstadt-Sigmaringen, Sigmaringen
Coating Design of Experiments Feste Darreichungsformen Prozessoptimierung Quality by Design Tabletten DoE Design of Experiments EMA European Medicines Agency FDA U.S. Food and Drug Administration FMEA Failure Mode and Effects Analysis HPMC Hydroxypropylmethylcellulose ICH International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use OFAT One-factor-at-a-time method QbD Quality by Design SOP Standard Operating Procedure In der pharmazeutischen Herstellung und Qualitätssicherung stellt die Prozessoptimierung eine wesentliche Säule dar. Dabei finden Prozessoptimierungen sowohl in der Entwicklung neuer Produkte, aber auch in deren Weiterentwicklung und Verbesserung statt. Die folgenden Ausführungen zeigen, am Beispiel eines Tablettencoatingprozesses, die Anwendung eines Quality by Design (QbD) – Ansatzes. Mit diesem wurden ...
-
19. GMP-Konferenz: GMP und GDP Update
Rubrik: Tagungsberichte
(Treffer aus pharmind, Nr. 02, Seite 267 (2014))
Schnettler R | Müller I | Junker R
19. GMP-Konferenz: GMP und GDP Update / Bericht von einer Konferenz der Hochschule Albstadt-Sigmaringen mit der DGGF (Deutsche Gesellschaft für Gute Forschungspraxis e. V.) und PTS Training Service am 03./04. Dezember 2013 in Düsseldorf · Schnettler R, Müller I, Junker R · PTS Training Service, Arnsberg und Hochschule Albstadt-Sigmaringen
Als erster Referent der Konferenz sprach Dr. Christian Jäkel (Fachanwalt der Kanzlei Dr. Jäkel, Lübben) über die neuesten Entwicklungen des Arzneimittelrechts. Im Mittelpunkt stand das dritte Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 07.08.2013, BGBI. I, S. 3108. Die wichtigsten Änderungen und Ergänzungen der sogenannten AMG-Novelle betreffen: die neue Anzeigepflicht „Nichtvermarktung“ Anzeigepflicht erweitert: PASS/AWB AM-HandelsV: Prüfpflicht Arzneimittellieferung in Nicht-EU/EWR-Staaten. Nach § 29 Abs. 1 g AMG hat der Inhaber der Zulassung seit Inkrafttreten am 28.10.2013 eine unverzügliche Anzeigepflicht bei „Nichtvermarktung“ von Arzneimitteln gegenüber der zuständigen Bundesoberbehörde. Diese Änderung gilt nur für Humanarzneimittel. In Anlehnung an die Pharmakovigilanz-Richtlinie sind Gründe für das vorübergehende oder endgültige ...
-
Jahre vergehen, Funktionen bestehen
Rubrik: Automation
(Treffer aus TechnoPharm, Nr. 06, Seite 346 (2013))
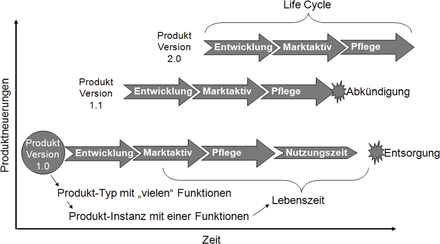
Jahre vergehen, Funktionen bestehen / Schade • FDT Standards · Schade M · Weidmüller Interface GmbH & Co. KG, Detmold
Life-Cycle-Management FDT2 Life Cycle Policy Die Verfügbarkeit von Produkten über ihre gesamte Nutzungszeit gewinnt in der Automatisierungstechnik immer mehr an Gewicht. Die FDT Group und Ihre Mitgliedsfirmen handhaben dies zukunftsgerecht durch den effizienten Einsatz von Life-Cycle-Management-Richtlinien. Der reine Lebenszyklus eines Produktes reicht von seiner Markteinführung bis zur Abkündigung. Einmal eingesetzt, überdauern Produkte ihren eigenen Lebenszyklus jedoch zum Teil noch Jahrzehnte, bis sie schließlich entsorgt werden. Wie wird in dieser Zeit sichergestellt, dass bei dem Austausch eines Produktes weiterhin die Verfügbarkeit des Gesamtsystems gegeben ist? Wie bleiben eingerichtete Funktionen erhalten? Die FDT Group Mitgliedsfirmen begegnen dieser Herausforderung durch die Integration von ...
-
Es gibt 11 weitere Treffer zu Ihrer Anfrage[ Alle Treffer dieser Rubrik anzeigen ]