Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Gutmann H.
In der Rubrik Zeitschriften haben wir 3 Beiträge für Sie gefunden
-
Prüfmittelmanagement im GxP-regulierten Umfeld
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 01, Seite 26 (2023))
Gutmann H | Meister M | Spiller S
Prüfmittelmanagement im GxP-regulierten Umfeld / Anforderungen & Umsetzung – Teil 2*Teil 1 dieses Beitrags ist erschienen in TechnoPharm 12, Nr. 5, 254-258 (2022). · Gutmann H, Meister M, Spiller S · Testo Industrial Services GmbH, Kirchzarten
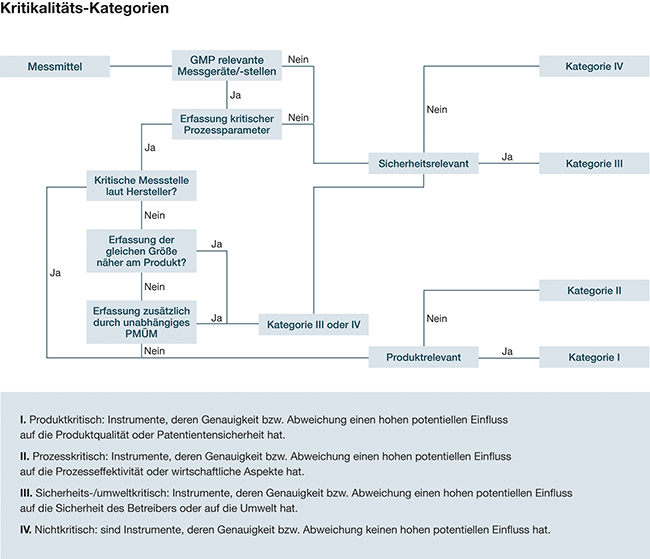
Bevor die Prüfmittelidentifizierung und die Messtellenrisikoanalyse inklusive der Kalibrierintervallbestimmung vorgenommen werden, sollten vorab Einstufungskriterien für die Bestimmung der Kritikalität der Messmittel festgelegt werden. Mit gut durchdachten Kriterien muss später bei Neuanschaffungen von Messmitteln der Einstufungsprozess nicht jedes Mal neu gestartet werden und der Bearbeitungsaufwand verringert sich. Hierbei ist zu beachten, dass zu grobe Betrachtungen, wie das Auslassen (in der Betrachtung) eines nachgeschalteten Prozesses, zu einer möglicherweise zu „harten“ Eingruppierung (Klasse I statt II) führen könnten, wodurch der wirtschaftliche Vorteil und die Effizienz des Entscheidungsschemas wieder verringert werden würden. Abbildung 2 zeigt ein mögliches Beispiel für ein solches Einstufungsschema. Hier wird durch Ja/Nein-Fragen die ...
-
Prüfmittelmanagement im GxP-regulierten Umfeld
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 05, Seite 254 (2022))
Gutmann H | Meister M | Spiller S
Prüfmittelmanagement im GxP-regulierten Umfeld / Anforderungen & Umsetzung – Teil 1 · Gutmann H, Meister M, Spiller S · Testo Industrial Services GmbH, Kirchzarten
GxP-konformes Prüfmittelmanagement Kalibriermanagement GAMP Automatisierte Prüfmittelmanagementsysteme Ein funktionierendes Prüfmittelmanagementsystem und ein effizientes Kalibriermanagement sind nicht nur Voraussetzung für richtige Messungen und damit korrekte Entscheidungen in einem Unternehmen, sondern auch eine grundlegende Anforderung aus dem Qualitätsmanagement. Das Prüfmittelmanagement berücksichtigt dabei den gesamten Lebenszyklus des Messmittels – von der Beschaffung bis hin zur Außerbetriebnahme. Innerhalb dieses Lebenszyklus bildet die regelmäßige Rekalibrierung den Schlüssel für eine geeignete metrologische Rückführung. Die große Bedeutung dieser Thematik spiegelt sich in allen relevanten Qualitätsmanagementnormen und -leitfäden des Good-Manufacturing-Practice(GMP)-Compliance-Umfelds wider. In der ISO 9001:2015 [1] wird im Kapitel „Ressourcen zur Überwachung und Messung“ die grundlegende Forderung nach einem systematischen ...
-
Kalibrierung als Basiselement der Qualitätssicherung in GMP-regulierten Bereichen
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 02, Seite 108 (2021))
Gutmann H | Kopf M | Salemink M | Sander C
Kalibrierung als Basiselement der Qualitätssicherung in GMP-regulierten Bereichen / Gutmann et al. • Kalibrierung · Gutmann H, Kopf M, Salemink M, Sander C · Testo Industrial Services, Kirchzarten und
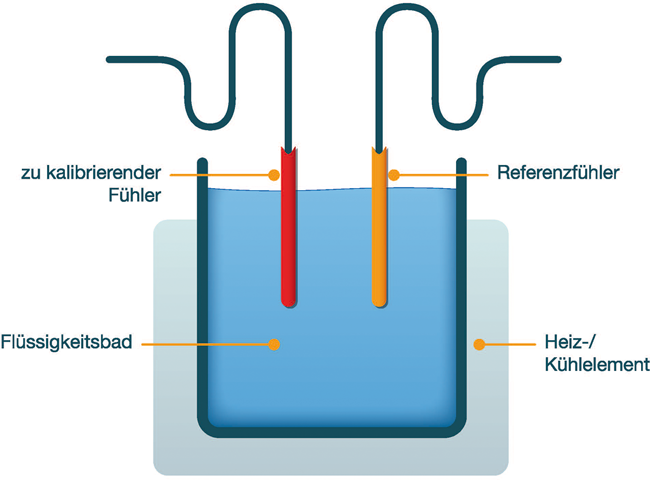
Kalibrierung Kalibriermanagement Messunsicherheit Konformitätsbewertung Qualitätssicherung In der Arzneimittelherstellung spielen Daten und deren Erhebung eine Schlüsselrolle. Vom Eingang der Rohstoffe bis zur Endfreigabe des Fertigprodukts werden immer wieder Ergebnisse (Ist-Werte) mit Spezifikationen (Soll-Werte) abgeglichen, um zu entscheiden, ob die Qualität den Anforderungen entspricht. Dies gilt gleichermaßen für Messwerte im Herstellungsprozess als auch für Ergebnisse im Labor. Messwerte entscheiden also über Akzeptanz oder Zurückweisung von Ausgangsstoffen, Zwischenprodukten und Endprodukten. Auf Messwerte muss Verlass sein – nur richtige (Mess-)Werte führen zu richtigen Entscheidungen. Deshalb muss in der pharmazeutischen Industrie die gesamte qualitätsrelevante Messtechnik kalibriert werden. Qualitätsrelevant ist Messtechnik, auf Basis derer Ergebnisse Entscheidungen ...