Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12022 Beiträge für Sie gefunden
-

Verpackungsreihe CEeasy stützt Drei-Punkte-Konzept
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 112 (2014))
Verpackungsreihe CEeasy stützt Drei-Punkte-Konzept / Produkte
Anwenderfreundliche Verpackungen gelten als eine wirksame Maßnahme, Patienten bei der verordnungsgemäßen Einnahme von Medikamenten zu unterstützen. Die internationale Verpackungsgruppe Edelmann *) hat darauf mit einem Drei-Punkte-Konzept reagiert, auf dem die Verpackungsreihe CEeasy basiert. Jedes Jahr könnten die Gesundheitsausgaben um durchschnittlich 19 Milliarden Euro geringer ausfallen, so die Zahlen von IMS. Die Kosten, die durch mangelnde Therapietreue entstehen, machen mit 13 Milliarden Euro den größten Anteil aus. Insbesondere bei chronischen Krankheiten kommt es laut Weltgesundheitsorganisation häufig vor, dass Patienten ihre Medikamente nicht wie vom Arzt verordnet einnehmen, sie vergessen oder die Einnahme abbrechen. Anwendungsfreundlich gestaltete Verpackungen können die Compliance und ... -
Supply Chain Visibility in der Pharmabranche
Rubrik: Logistik
(Treffer aus TechnoPharm, Nr. 02, Seite 102 (2014))
Supply Chain Visibility in der Pharmabranche / Chancen und Grenzen neuester Gesetze und Technologien · Krebs T, Schön A · Miebach Consulting GmbH
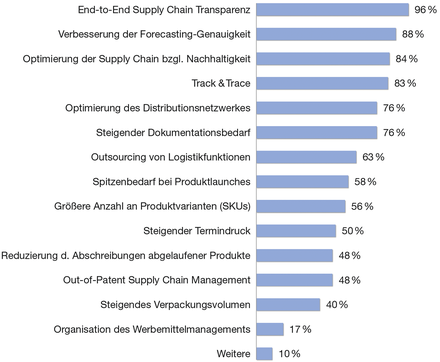
Supply Chain Visibility ist ein wesentlicher Baustein, mit dem Pharmaunternehmen die erforderliche Transparenz schaffen, um global vernetzte Lieferketten mit ihren physischen Warenflüssen und informatorischen Datenströmen nachverfolgen und steuern zu können. Vielen Pharmaunternehmen ist es allerdings noch nicht in Gänze „auf Knopfdruck“ möglich, ein klares Bild über die aktuellen Beschaffungs- und Distributionsvorgänge zu erhalten. Die Optimierung hin zur vollständigen End-to-End-Supply-Chain-Transparenz steht daher auf Platz 1 der Optimierungsthemen für Entscheider in der Pharmaindustrie, so das Ergebnis der Miebach-Studie von 2012 über Supply-Chain-Trends in der Pharmabranche (siehe Abb. 1 ). So gaben 96 % der Studienteilnehmer als wichtigstes Thema der Pharmalogistik die End-to-End-Supply-Chain-Transparenz an. 88 % ...
-
Screening-Methoden zur Bewertung der Delaminationsneigung von Primärverpackungen
Rubrik: Analytik
(Treffer aus TechnoPharm, Nr. 02, Seite 99 (2014))
Screening-Methoden zur Bewertung der Delaminationsneigung von Primärverpackungen / Haines • Screening-Methoden zur Bewertung der Delaminationsneigung · Haines D · SCHOTT Pharmaceutical Systems, SCHOTT pharma services, SCHOTT North America, Duryea, PA (USA)
Um die Ursachen der Glas-Delamination früh zu erkennen und ihnen entgegenzuwirken, muss man zunächst verstehen, wie sich Glas chemisch zusammensetzt, welche Produktionsprozesse die Behälter durchlaufen und wie Medikamente mit Glasoberflächen chemisch reagieren. Zudem gilt: Pharmazeutische Behälter, selbst wenn sie aus demselben Typ 1 Glas bestehen, können sich signifikant unterscheiden. So führen Unterschiede in der chemischen Zusammensetzung (um bis zu 10 Gewichtsprozent einzelner Elemente) auch zu unterschiedlichem physikalischen Verhalten. Dies betrifft hauptsächlich die Schmelz- und Arbeitstemperaturen, da Behälter mit höherem Siliziumgehalt (Typ 1A Glas) höhere Produktionstemperaturen erfordern. Die Mehrzahl pharmazeutischer Verpackungen besteht entweder aus Hütten- oder aus Röhrenglas. Hüttenglas weist chemisch ...
-
Etikettieranlagen in Modulbauweise
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 92 (2014))
Etikettieranlagen in Modulbauweise / Im Pharmaumfeld fit für Spezialaufgaben · Fischer U · HERMA GmbH, Deizisau
Kaum eine Branche muss sich inzwischen so komplexen Anforderungen bei Produktinformation und Kennzeichnung stellen wie die pharmazeutische Industrie. Dabei ist der pure Umfang der Information – obwohl er inzwischen auch schon ein beträchtliches Maß erreicht hat – nur ein Thema unter vielen. Die absolut zuverlässige Sicherstellung der Kennzeichnung, die lückenlose Rückverfolgbarkeit, Maßnahmen gegen Produktfälschungen und spätestens ab 2017 auch die EU-weit vorgeschriebene Serialisierung sind weitere Aspekte, die heute jeden Produktionsleiter vor gewaltige Aufgaben stellen. Eine Fülle von unterschiedlichen Technologien – für Druck, Identifikation, Etikettierung und Kontrolle – muss auf engstem Raum, nämlich in der eigentlichen Etikettieranlage, so zusammenspielen, dass auch ...
-
Lasertechnologie: Multitalent an der Verpackungslinie
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 88 (2014))
Lasertechnologie: Multitalent an der Verpackungslinie / Müller • Lasertechnologie: Multitalent an der Verpackungslinie · Müller U · KBA Metronic GmbH, Veitshöchheim
Gefälschte Medikamente sind eine Gefahr für die Gesundheit der Konsumenten und verursachen finanzielle Verluste bei den Herstellern. Deshalb legen die Pharmaunternehmen höchsten Wert darauf, die Fälschungssicherheit ihrer Produkte zu gewährleisten. Das geschieht in Form von Daten, die einzelne Artikel eindeutig zuordenbar machen. Daneben gilt es auch, Verfallsdaten dauerhaft aufzubringen, damit z. B. Medikamente mit begrenzter Haltbarkeit nicht nach dem Verfallsdatum eingenommen werden. Eine bewährte Lösung, diese Informationen aufzubringen, ist die Laserkennzeichnung. Mit ihr lassen sich unterschiedliche Oberflächen sowohl im Stillstand als auch in der Bewegung dauerhaft und abriebfest markieren oder beschriften. Dabei kann eine Vielzahl von Materialien gekennzeichnet werden, einschließlich Papier, ...
-
Packmittel-Alternativen für Systeme mit Delaminationsneigung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 84 (2014))
Packmittel-Alternativen für Systeme mit Delaminationsneigung / Hladik • Packmittel-Alternativen für Systeme mit Delaminationsneigung · Hladik B · SCHOTT Pharmaceutical Systems, Mainz
Um eine möglichst homogene Innenoberfläche des Packmittels gewährleisten und dadurch seine chemische Beständigkeit verbessern, gibt es zwei prinzipielle Lösungsansätze: Eine Variante ist eine in einem Plasmareaktor generierte homogene Innenoberflächen-Beschichtung aus Siliciumdioxid. Dabei werden die Fläschchen zunächst gewaschen und dann in einem Wärmetunnel getrocknet. Anschließend kommen die Behältnisse in einen Plasma-Reaktor. In dem gepulsten Plasmaverfahren werden mehrere Siliciumdioxid-Lagen an der inneren Oberfläche der Behältnisse aufgebracht. Die homogene Schicht ist transparent und weist sehr gute Barriereeigenschaften auf. Die Behälter können in allen gängigen pharmazeutischen Verfahrensschritten wie Waschen, Autoklavieren, Sterilisieren oder Depyrogenisieren bei Temperaturen bis zu 350° C eingesetzt und wie unbeschichtete Fläschchen gefüllt, ...
-
Eindeutig und fälschungssicher
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 78 (2014))
Eindeutig und fälschungssicher / In großen Schritten zur neuen Pharmacodierung · Hähn M · GS1 Germany GmbH, Bereich GS1 Standards & Products, Köln
Wegweisende Entwicklungen in der Pharmabranche zeichnen sich ab: Mit Verabschiedung der EU-Richtlinie 2011/62/EU wurde der Grundstein für eine größere Patientensicherheit in Europas und damit auch in deutschen Apotheken gelegt. Der wesentliche Punkt der Direktive betrifft die Einführung von europaweit harmonisierten Sicherheitsmerkmalen, anhand derer die Verifizierung und Authentifizierung von Arzneimitteln ermöglicht wird. Diese Sicherheitsmerkmale sollen von den Herstellern auf den Packungen aufgebracht werden und es Großhändlern und Apothekern erlauben, deren Echtheit zu überprüfen und Manipulationen der äußeren Umhüllung zu erkennen. Da es sich hier um einzelne Packungen dreht, reicht die Identifikation des Arzneimittels über die in Deutschland gültige Pharmazentralnummer (PZN) als ...
-
Sicherheitsmerkmale für Medikamentenfaltschachteln
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 72 (2014))
Sicherheitsmerkmale für Medikamentenfaltschachteln / Herausforderungen für Etikettiersysteme · Kästing U · MULTIVAC Marking & Inspection GmbH & Co. KG, Enger
Die Europäische Union kämpft seit Jahren gegen Arzneimittelfälschungen. Mitte Juli 2011 hat sie dazu eine neue Richtlinie (2011/62/EU) auf den Weg gebracht. Zum Schutz von Patienten und Verbrauchern müssen Medikamentenpackungen in naher Zukunft mit einem individuellen Erkennungsmerkmal und einem Fälschungsschutz versehen sein. Wer aus Effizienz- und Kostengründen eine Lösung sucht, mit der sich beide Merkmale in einem Prozessschritt integrieren lassen, könnte den Einsatz spezieller Etikettiersysteme in Erwägung ziehen. Mit ihnen lassen sich manipulationssichere Siegeletiketten auf den Medikamentenfaltschachteln anbringen und eine eindeutige Seriennummer in Form eines seriellen Codes (DataMatrix-Code) aufdrucken. Kennzeichnungssysteme bieten in diesem Zusammenhang etliche Vorteile: So ist beispielsweise das ...
-
GMP- und reinraumgerechte Verpackungen – Grundlagen
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 64 (2014))
GMP- und reinraumgerechte Verpackungen – Grundlagen / Verpackung als Kontaminationsrisiko · Strubl C · STRUBL KG, D Wendelstein
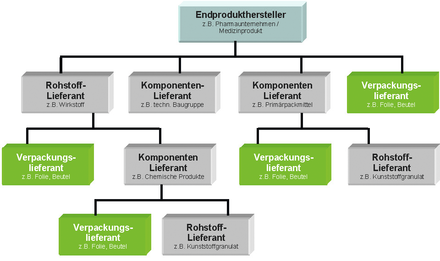
In den letzten Jahren nimmt die Anzahl an Messen, Konferenzen und spezifischen Fachorganen im Umfeld der Themen GMP und Reinraum ständig zu [ 1 ]. Verursacht wird dieser Trend von der allgemein positiven wirtschaftlichen Entwicklung des Medizintechnik- und Pharmasektors. Aktuelle Studien prognostizieren für Pharmaverpackungen ein globales Marktwachstum um jährlich ca. 6,4 % bis zum Jahr 2017 [ 2 ]. Neben der steigenden Nachfrage ist ein wesentlicher Impulsgeber für diese Entwicklung vor allem in den sich verschärfenden Regulationsanforderungen in den Branchen Pharma und Medizintechnik zu sehen. Inzwischen gibt es praktisch keinen Bereich in der Lieferantenumwelt der Endproduktehersteller, der sich nicht mit den ...
-

Packmittel: Vom Streben nach Perfektion
Rubrik: Editorial
(Treffer aus TechnoPharm, Nr. 02, Seite 1 (2014))
Packmittel: Vom Streben nach Perfektion / Editorial
Wenn es die TechnoPharm 2-2014 auf Ihren Schreibtisch geschafft hat, dann ist es nicht abwegig, dass sich Zug- oder Flugticket zur Düsseldorfer „interpack“ ebenfalls in Griffweite befinden. Und wie Ihnen geht es schätzungsweise 170 000 Anderen. Von nah und fern reisen sie an, um auf dem gut 300 000 qm 2 großen Gelände die neuesten Trends und Innovationen der Verpackungsindustrie zu bestaunen. Die Messe hat für dieses Jahr ca. 2700 Aussteller angekündigt. Doch wussten Sie, dass die „interpack“ dieses Jahr 20-jähriges Jubiläum feiert? Wir nicht. Was vor allem der Tatsache geschuldet ist, dass die erste Messe – bedingt durch den 3-Jahres-Turnus – ...
Sie sehen Artikel 6281 bis 6290 von insgesamt 12022
- Erste Seite
- 627
- 628
- 629
- 630
- 631
- Letzte Seite