GKV-Spargesetz: Eine „Katastrophe“ für Menschen mit Schmerzen
03.06.2026Die Deutsche Schmerzgesellschaft geht davon aus, dass durch das GKV-Beitragssatzstabilisierungsgesetz (BStabG) die Versorgung von Millionen chronisch schmerzkranken Menschen massiv gefährdet ist. ...
14 Gründungsteams in drei Jahren: Weitere Förderung für Healthcare Accelerator in Regensburg
02.06.2026Die BioPark Regensburg GmbH, ein Unternehmen der Stadt Regensburg, erhält eine weitere Förderung vom Bayerischen Staatsministerium für Wirtschaft, Landesentwicklung und Energie. Bayerns ...
Haben Apotheken Zukunft?
01.06.2026Der Markt der Arzneimittelversorgung befindet sich im Wandel. Neben den klassischen Vor-Ort-Apotheken treten zunehmend neue Anbieter auf – von nationalen und internationalen Versandapotheken bis ...
Karl Landsteiner Privatuniversität startet neues internationales PhD Programm für Krebsforschung
03.06.2026Die Karl Landsteiner Privatuniversität erweitert ihr internationales Forschungsprofil um ein neues Doktoratsprogramm: Das englischsprachige PhD-Programm „TUMOR BIOLOGY: Basic, Translational, and ...
meistgelesen
Beitrag aus der Ausgabe 1/2026 der Zeitschrift pharmind
Stabilitätsprüfung von Wirkstoffen und Arzneimitteln
Der Entwurf der neuen ICH-Leitlinie Q1
Stabilitätsuntersuchungen sind ein essenzieller Bestandteil der Arzneimittelentwicklung und -zulassung. Sie dienen dazu, die Qualität, Sicherheit und Wirksamkeit eines Arzneimittels über einen definierten Zeitraum, die Verwendbarkeitsfrist, zu gewährleisten. Die Bedeutung wird auch dadurch verdeutlicht, dass die Stabilitätsleitlinie Q1A „Stability Testing of New Drug Substances and Products“ das erste Thema war, welches im ...
Beitrag aus der Ausgabe 4/2025 der Zeitschrift Tech4Pharma
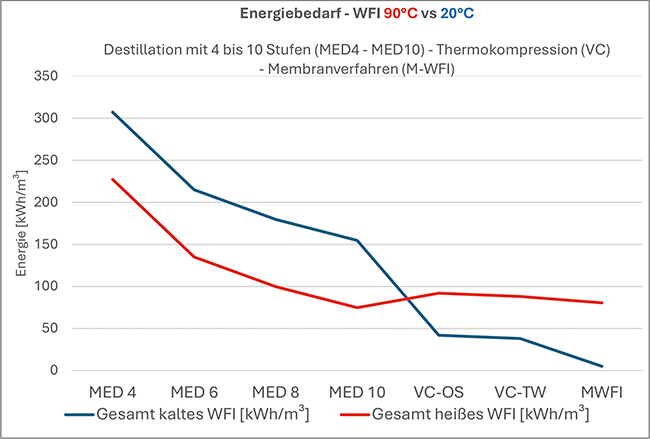
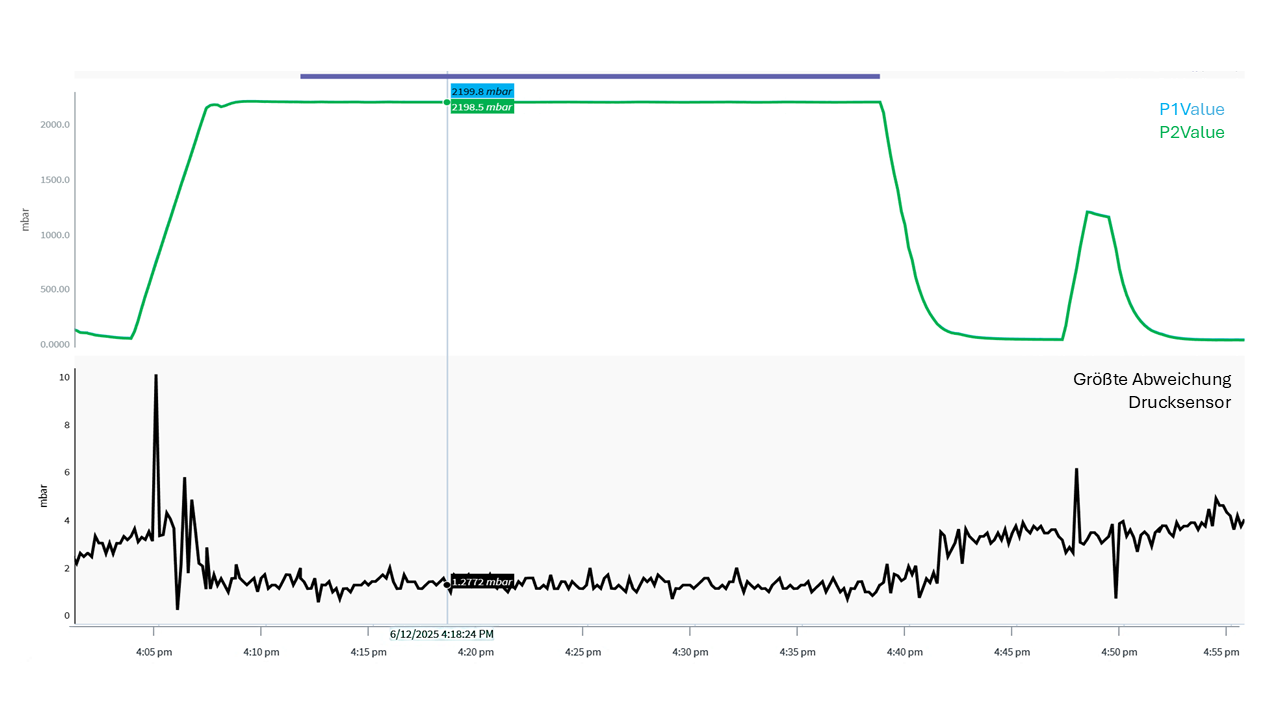
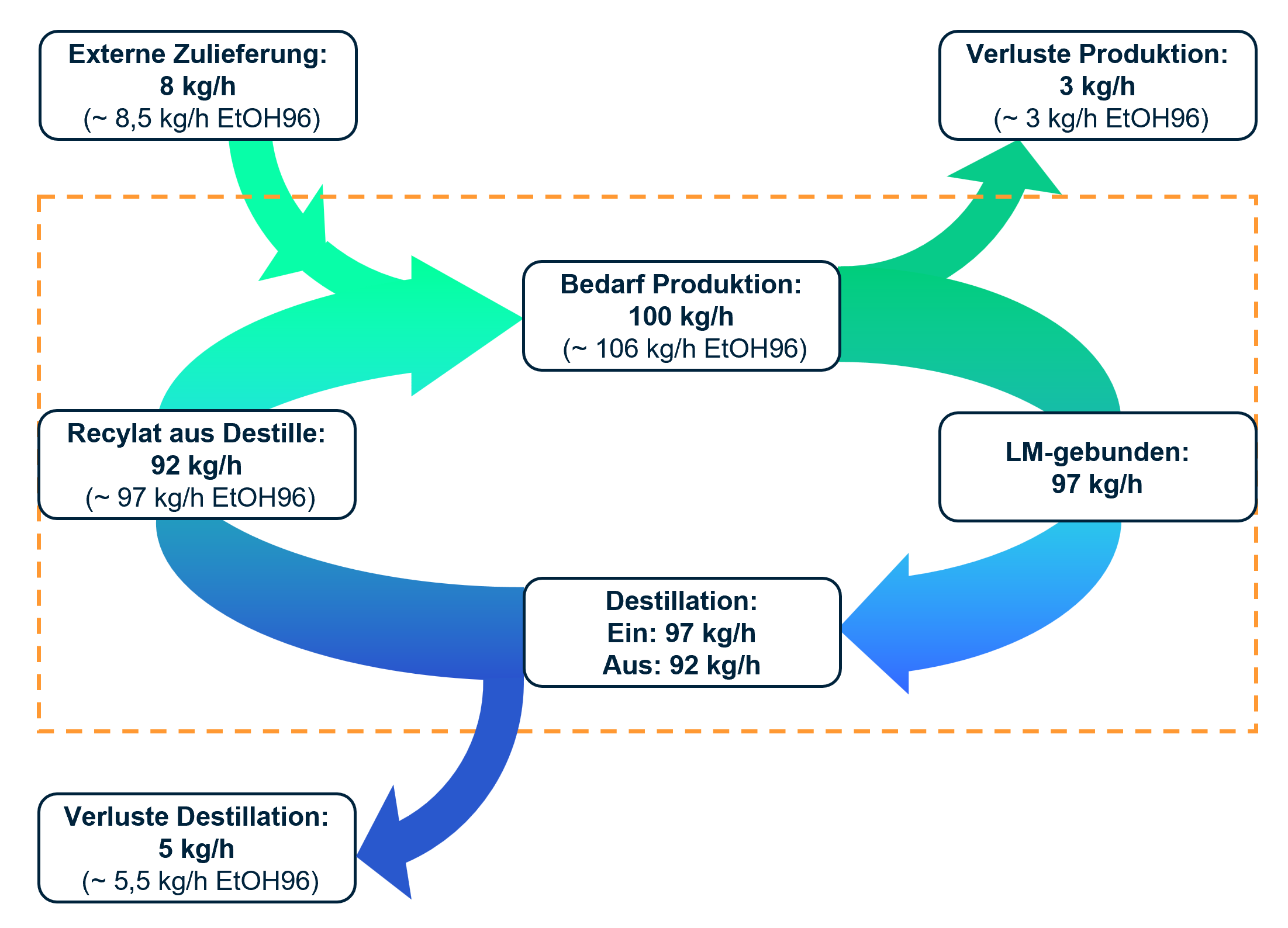
Serie: Energetische Analyse von WFI-Systemen
Teil 2*Teil 1 dieser Serie s. Tech4Pharma 2025;15(3):158–163.: WFI-Erzeugung – Auswahlkriterien und Energiebilanz
Der erste Serienteil bot einen Überblick über die gängigen Verfahren zur Herstellung von Wasser für Injektionszwecke (WFI): Mehrstufendestillation, Thermokompression und membranbasierte Systeme. Die Funktionsweise, Betriebsmöglichkeiten und energetischen Eigenschaften der Technologien wurden systematisch dargestellt. Ein besonderer Fokus lag auf Nachhaltigkeitsaspekten und integrierten Energiesparmaßnahmen.Im dritten Serienteil werden die ...
Beitrag aus der Ausgabe 2/2026 der Zeitschrift cleanroom & processes
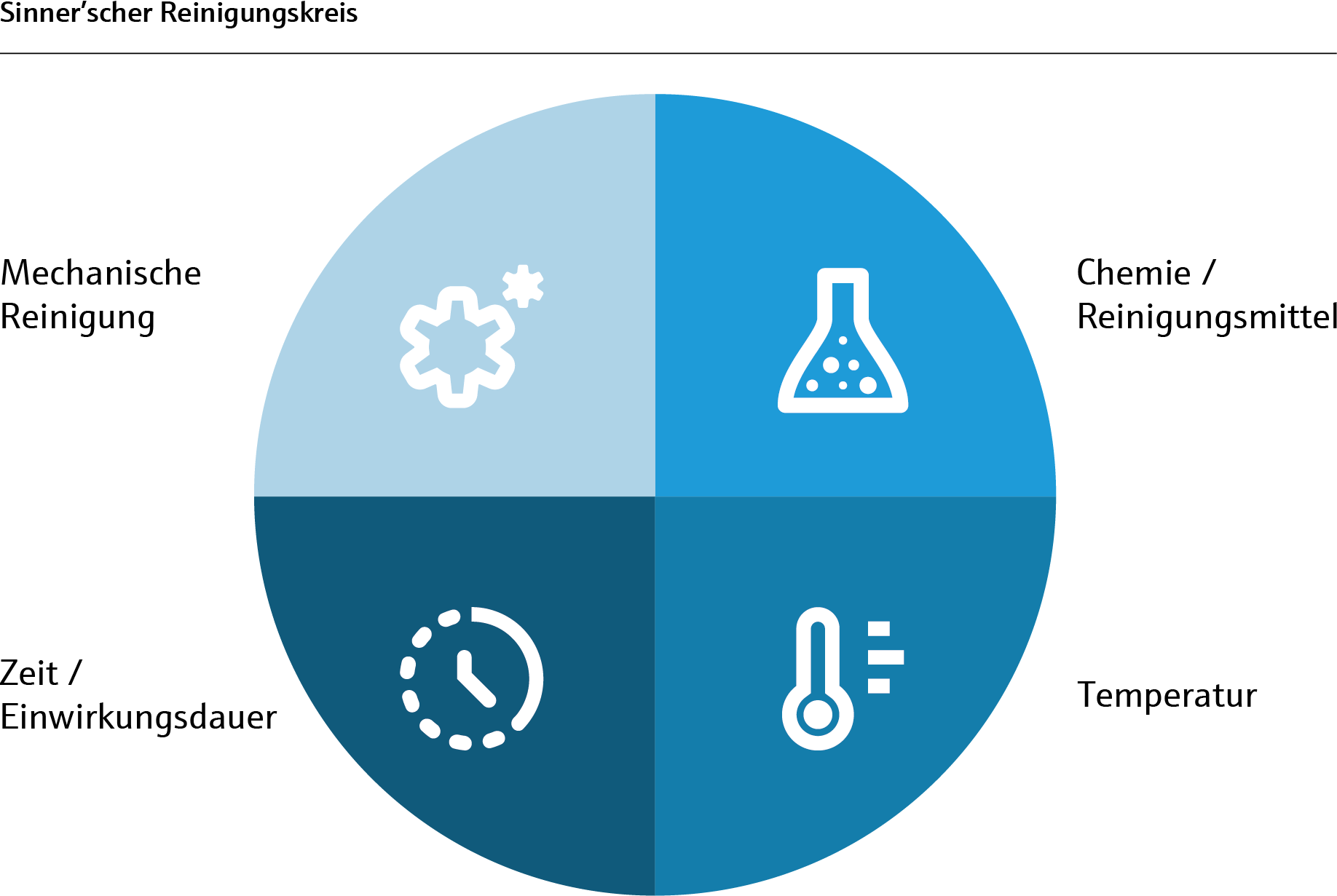
Schnee statt hochreinem Wasser
Medizin- und Pharmaprodukte sicher und ressourcenschonend reinigen
Das Spektrum an medizintechnischen Produkten und pharmazeutischen Erzeugnissen, die verpackt werden müssen, ist enorm vielfältig und stellt besondere Anforderungen an die Reinigung während der Herstellung. Dabei ist ein produktspezifisch definiertes Reinheitslevel zuverlässig zu erfüllen. Hinzu kommen regulatorische Vorgaben, die eingehalten werden müssen. Entsprechend ist ein Reinigungsprozess dann für die Herstellung von Medizintechnik- und ...
Top Themen
Beitrag aus der Ausgabe 5/2026 der Zeitschrift pharmind
Innovationsbooster European Biotech Act
Chancen und Herausforderungen
Der Mitte Dez. 2025 veröffentlichte Vorschlag für einen Biotech Act geht zurück auf eine Kommissionsmitteilung vom März 2024, in der erstmals ein neuer Rechtsrahmen zur Förderung der Biotechnologie für erforderlich gehalten wurde. [1] Kommissionspräsidentin von der Leyen hat diesen Gedanken in ihre im Juli 2024 vorgestellten politischen Leitlinien übernommen und einen Vorschlag für einen Biotech Act angekündigt. Danach soll dieser neue Rechtsakt ...

Beitrag aus der Ausgabe 2/2026 der Zeitschrift Tech4Pharma
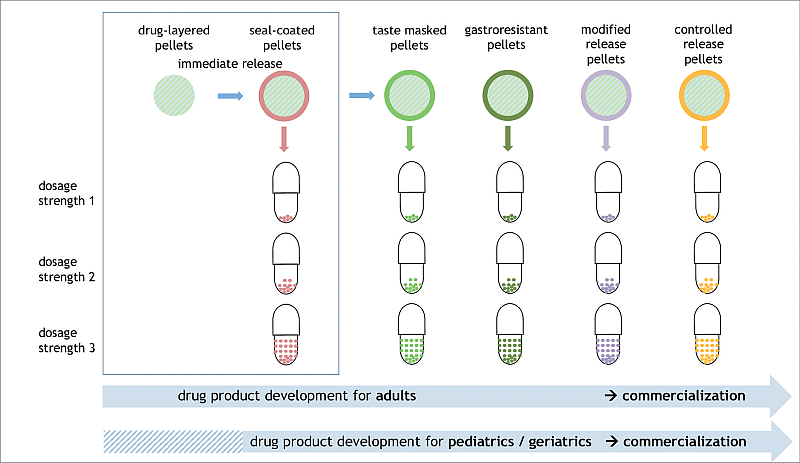
Einstieg in Continuous Manufacturing
Technologische, prozessuale und entwicklungsrelevante Aspekte der kontinuierlichen Feuchtgranulation
In der Pharmaindustrie werden Granulationsprozesse zunehmend unter den Aspekten der Effizienzsteigerung und Kostenoptimierung betrachtet. Ziel der Feuchtgranulation ist es, aus feinem Pulver gröbere Agglomerate zu erzeugen. Agglomerate können aus festen und trockenen Körnern bestehen, wobei jedes Korn ein Agglomerat aus Pulverpartikeln mit genügend Festigkeit darstellt. Granulate können direkt als Arzneimittel verwendet werden oder dienen als ...

Beitrag aus der Ausgabe 2/2026 der Zeitschrift cleanroom & processes
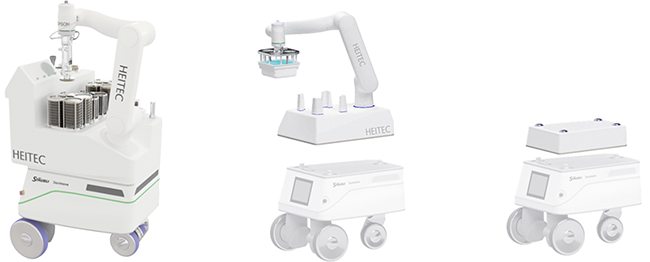
Innovationen im pharmazeutischen Reinraum
Kontaktlose Authentifizierung, mobile Robotik und intelligente Bedienkonzepte für die Pharmaproduktion
In hochreinen Produktionsbereichen der Pharmaindustrie steht die Vermeidung von Kontaminationen an oberster Stelle. Das größte Risiko geht dabei vom Menschen aus, weshalb Reinräume nur von autorisiertem Fachpersonal betreten werden dürfen. Gleichzeitig erfordern moderne Herstellprozesse eine lückenlose Kontrolle und Dokumentation, um Qualität und Compliance – etwa mit den GMP-Regularien – sicherzustellen. Traditionelle Verfahren ...

Vorschau (Änderungen vorbehalten)
Beitrag aus der nächsten Ausgabe 6/2026 der Zeitschrift pharmind
(erscheint am 30.06.2026)
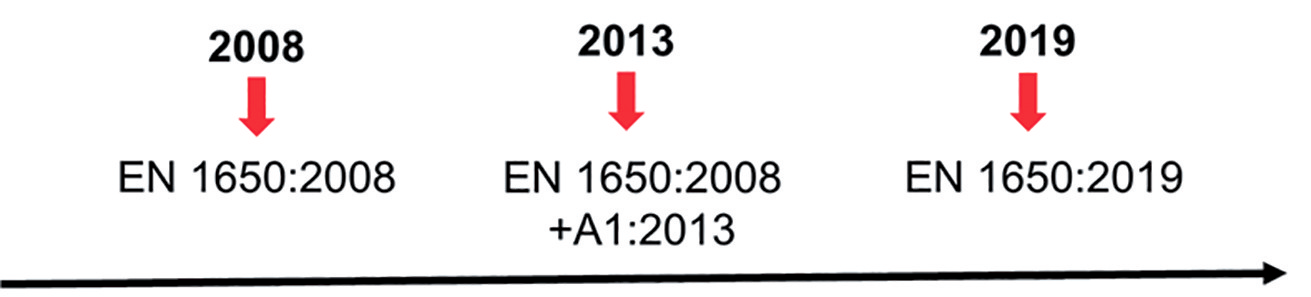
Fungicidal efficacy of alcoholic disinfectants | Impact of cultivation of Aspergillus brasiliensis
To be used as disinfectants in Europe, biocidal products such as alcoholic disinfectants are regulated by the EU’s Biocidal Product Regulation (BPR) EU No. 528/2012. Due to varying lengths of authorization procedures under the BPR, EN (European Norm) methods may change during the evaluation of BPR product authorizations, which may result in different antimicrobial efficacy claims for identical formulations such as 70 % (v/v) propan-2-ol. In this study, we investigated the impact of cultivation of A. brasiliensis established in EN 1650 in 2013 compared to the previous version of EN 1650 on fungicidal efficacy against A. brasiliensis.

Beitrag aus der nächsten Ausgabe 3/2026 der Zeitschrift Tech4Pharma
(erscheint am 09.09.2026)
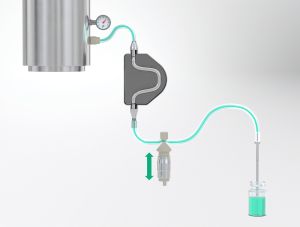
Fülltechnologie für flüssige, sterile Formen / Rüsten – Betreiben – Füllsystemtypen und deren Eigenschaften – Teil 2
Im ersten Teil dieses Fachbeitrags wurden die regulatorischen Vorgaben für das Abfüllen flüssiger Pharmazeutika sowie das aseptische Rüsten gemäß des EU-GMP Annex 1 erläutert. Weiterhin wurden die Grundlagen des Füllprozesses und das Strömungsverhalten von Fluiden beschrieben. Dieser zweite Teil behandelt den Aufbau und die Funktionsweise gängiger Fülltechnologien. Zusätzlich werden Möglichkeiten zur Reduktion von Produktverlust vor, während und nach der Produktion aufgezeigt. Abschließend werden Anforderungen verschiedener Produktklassen von Medikamenten erläutert sowie die damit einhergehende Wahl eines geeigneten Füllsystems begründet.


Beitrag aus der nächsten Ausgabe 03/2026 der Zeitschrift cleanroom & processes
(erscheint am 18.09.2026)
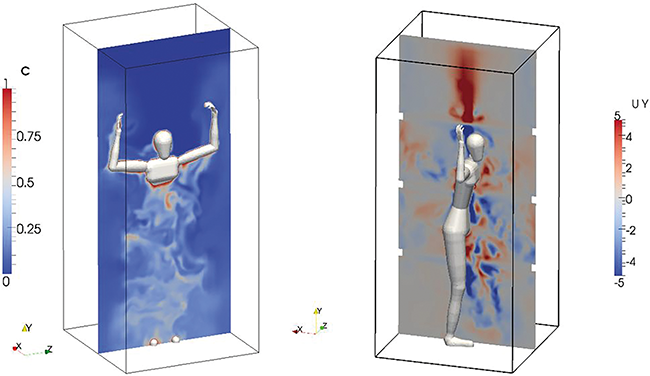
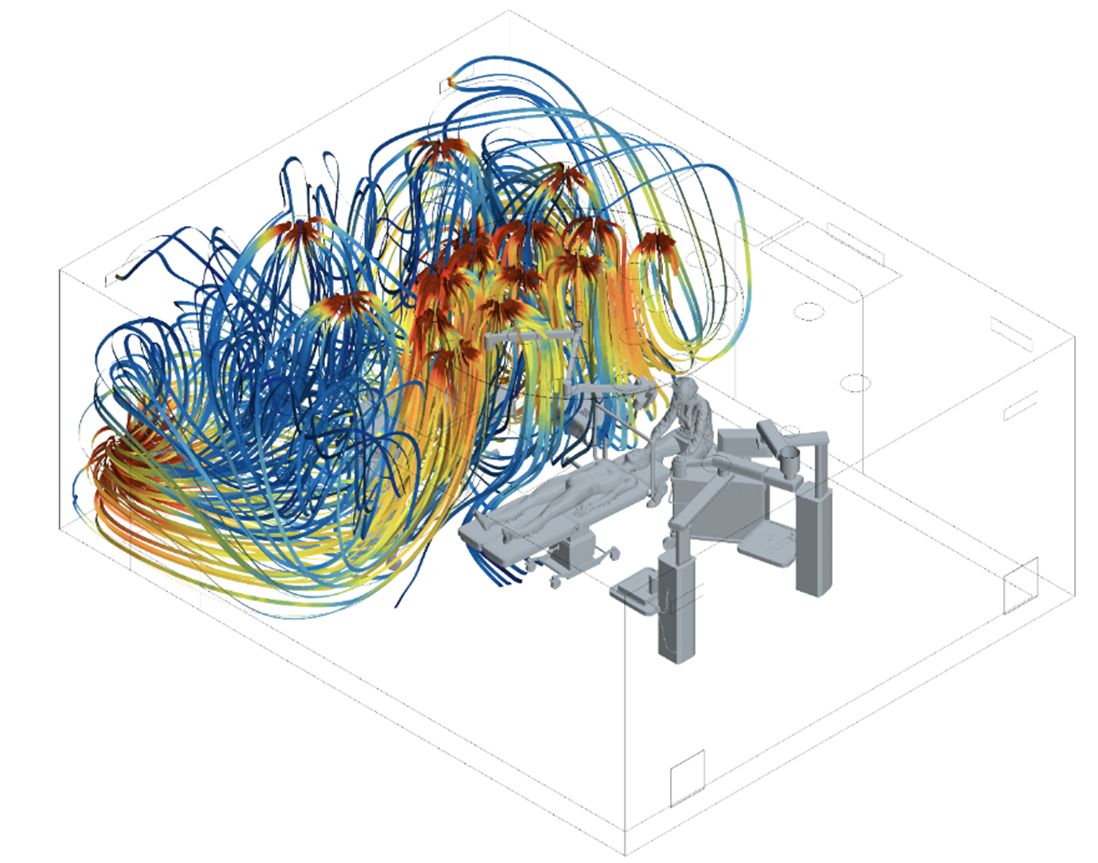
Trockenraum und Mensch - Wechselwirkungen und Beeinflussung
Die Produktion von Batteriezellen erfordert Rein- und Trockenräume mit hoher Partikelreinheit und extrem niedriger Luftfeuchte. Während die Technik solcher Umgebungen gut beschrieben ist, ist der Einfluss des Personals auf den Taupunkt sowie die Rückwirkung des trockenen Klimas auf die Mitarbeitenden kaum untersucht. Im Rein- und Trockenraumlabor des Fraunhofer IPA wurden Versuche zur durch Personen verursachten Veränderung des Taupunkts durchgeführt. Auf Basis der Ergebnisse wurden Verhaltensregeln sowie organisatorische und technische Maßnahmen abgeleitet, die sowohl die Stabilität des Trockenraumklimas als auch den Gesundheitsschutz unterstützen.