Cloud Provider und elektronische Signaturen | Beitrag aus pharmind 87 | Nr. 5 | Seite 472-477 (2025)
30.06.2025Dieser Beitrag behandelt die Rolle der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG) im Bereich der Arzneimittelüberwachung. Ein Schwerpunkt liegt auf ...
Evotec tritt dem NURTuRE-AKI-Konsortium bei, um ein multi-omics-basiertes molekulares Verständnis des akuten Nierenversagens zu erlangen
30.06.2025Evotec SE gab am 25.06.25 ihren Beitritt zum NURTuRE-AKI-Konsortium bekannt, um eine Patientenkohorte für akutes Nierenversagen (AKI), NURTuRE-AKI, aufzubauen. Diese Initiative ermöglicht es ...
Chemieverbände Rheinland-Pfalz: Schäfer als Vorsitzender bestätigt
30.06.2025Im Jubiläumsjahr wählen die Chemieverbände Rheinland-Pfalz ihren Vorstand neu. Sebastian Schäfer bleibt an der Spitze und betont Zusammenhalt in Zeiten der Transformation. In seiner Rede zur ...
Green-Claims-Richtlinie (GCD): Verbraucherschutz nicht doppelt regulieren!
30.06.2025Die Diskussion um die Green-Claims-Richtlinie (GCD) nimmt vor dem Hintergrund zunehmender Kritik aus Teilen des Europaparlamentes und aus den Mitgliedsstaaten weiter an Fahrt auf. In den letzten ...
meistgelesen
Beitrag aus der Ausgabe 1/2025 der Zeitschrift pharmind
Optimierung analytischer Methodentransfers
Eine herausfordernde Aufgabe und wie diese erfolgreich gemeistert werden kann
Analytische Transfers sind Aktivitäten, deren Einfluss auf die Routineanalytik nicht hoch genug eingeschätzt werden kann. Neben Aspekten des „reinen GMP“ sind die gewissenhafte inhaltliche Vorbereitung und erfolgreiche Durchführung auch ein wichtiger betriebswirtschaftlicher Aspekt, da eine unzuverlässige Analytik zu finanziellen Verlusten führen kann sowie unnötig Ressourcen im Abweichungsmanagement und bei der Fehlersuche bindet. ...
Beitrag aus der Ausgabe 12/2024 der Zeitschrift pharmind
Spezifische Prüfungen von Primärpackmitteln
Deister und Mendel | Prüfungen von Primärpackmitteln
Primärpackmittel kommen direkt mit dem zu verpackenden Arzneimittel in Kontakt. Daher ist ihnen bei der Packmittelprüfung besonders hohe Aufmerksamkeit zu widmen. Abhängig von der entsprechenden Darreichungsform und den arzneimittelspezifischen Anforderungen sind die verwendeten Packmittel sehr unterschiedlich (Abb. 1).Auch die Herstellungsverfahren der verschiedenen Packmittelkomponenten sind sehr unterschiedlich und komplex.Als Beispiel ...
Beitrag aus der Ausgabe 2/2025 der Zeitschrift pharmind
CMC und GMP – Update
Analytische Verfahrensentwicklung und Validierung in der Qualitätskontrolle – Teil 1
Die Entwurfsfassungen beider Leitlinien ICH Q2 „Guideline on validation of analytical procedures“ und ICH Q14 „Analytical Procedure Development“ wurden in zurückliegenden Beiträgen dieser Publikationsreihe bereits umfassend kommentiert [1,2]. Dabei wurden auch eine ganze Reihe von Inkonsistenzen dargestellt und Regelungsinhalte kommentiert, die man als nicht sachgerecht und/oder nicht dem Stand von ...
Branchenposter
Top Themen
Beitrag aus der Ausgabe 6/2025 der Zeitschrift pharmind
GxP-konforme Open-Source-Software für Pharma 4.0
Teil 1: Architektur und Design der Data Computation Platform
Die 4. industrielle Revolution, auch bekannt als Industrie 4.0, zielt darauf ab, die Information Technology (IT) und Operational Technology (OT) zu verbinden. Dadurch entstehen stark automatisierte und intelligente Produktionssysteme, die sowohl die Flexibilität als auch den Produktdurchsatz erhöhen und letztlich die Kosten senken [1]. Zudem fordern Gesundheitsbehörden pharmazeutische Hersteller auf, diesen neuen ...

Vorschau (Änderungen vorbehalten)
Beitrag aus der nächsten Ausgabe 7/2025 der Zeitschrift pharmind
(erscheint am 31.07.2025)
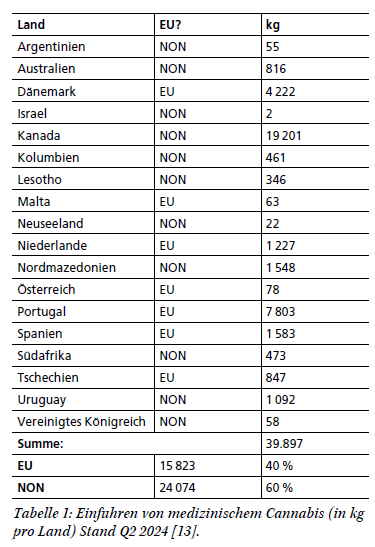
Cannabis-Logistik | Herausforderungen und Chancen nach Inkrafttreten des Medizinal-Cannabisgesetzes
Seit Apr. 2024 unterliegt die Verordnung von Cannabisarzneimitteln im Rahmen des Medizinal-Cannabisgesetzes (MedCanG) nicht länger dem Betäubungsmittelgesetz (BtMG) bzw. der Betäubungsmittelverschreibungsverordnung (BtMVV). Damit sind einige Anforderungen hinsichtlich Lagerung, Handling und Transport sowie der Abgabe von Cannabis-Produkten entfallen, jedoch können spezialisierte Logistikdienstleister aus dem Betäubungsmittelbereich bei der Vermeidung von gesetzlichen Fallstricken und Schwierigkeiten unterstützen. Der Beitrag blickt auf die Entwicklungen der Cannabis- und BtM-Logistik zurück und zeigt aktuelle Herausforderungen auf, mit Fokus auf dem Erhalt der MedCanG-Erlaubnis sowie dem Import aus dem Nicht-EU-Ausland.