Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Mang A.
In der Rubrik Zeitschriften haben wir 2 Beiträge für Sie gefunden
-
Etablierung eines systematischen Scale-Up-Prinzips im Life Cycle Management von Extrusionsprozessen
Rubrik: Prozesstechnik
(Treffer aus TechnoPharm, Nr. 04, Seite 196 (2020))
Etablierung eines systematischen Scale-Up-Prinzips im Life Cycle Management von Extrusionsprozessen / Mang und Fröhlich • Etablierung eines systematischen Scale-Up-Prinzips · Mang A, Fröhlich M · Abbvie Deutschland GmbH & Co. KG, Ludwigshafen
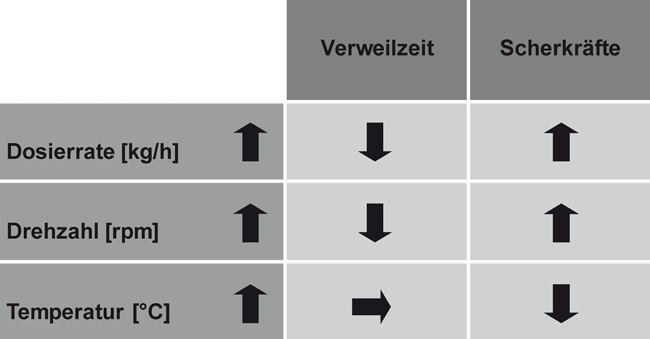
Extrusion Scale-Up Schwerlöslicher API Verweilzeitmessung Life Cycle Management Im Rahmen des Life Cycle Management von pharmazeutischen Herstellprozessen kann mit steigendem Marktbedarf ein Produkttransfer auf eine größere Produktionsanlage (Scale-Up) notwendig sein. Um diese Prozessänderung bei der European Medicines Agency (EMA) als geringfügige Änderung (Typ IA) zu registrieren, müssen identische Produktqualität, Sicherheit und Wirksamkeit nachgewiesen werden. Eine Abweichung von Produktspezifikationen, Inprozesskontrollen sowie Änderungen des Verunreinigungsprofils hätte hingegen eine umfassende Änderung (Typ II) zur Folge. Im folgenden Beitrag wird der Scale-Up eines Extrusionsprozesses für ein registriertes, kommerzielles Produkt beleuchtet. Dieser Scale-Up erfordert eine Anpassung von kritischen Prozessparametern (CPPs), die von der Größe des Extruders abhängig ...
-
Einsatz von Disposables in der Pharma-Parenteralia-Produktion
Rubrik: Originale
(Treffer aus pharmind, Nr. 11, Seite 1810 (2013))
Weitbrecht T | Kallmeyer G | Klotz U | Posset T | Mang A
Einsatz von Disposables in der Pharma-Parenteralia-Produktion / Weitbrecht et al. • Disposables in der Parenteralia-Produktion · Weitbrecht T, Kallmeyer G, Klotz U, Posset T, Mang A · Roche Diagnostics GmbH, Mannheim und
Extractables Leachables Parenteralia Pufferherstellung Single-Use Disposables Threshold of Toxicological Concern In den vergangenen Jahren fanden viele Disposable/Single-Use-Systeme ihren Einsatz in der biotechnologischen Wirkstoff-Herstellung [ 1 , 2 ]. Das liegt vor allem an den vielen Vorteilen dieser Systeme, die in der letzten Zeit immer mehr an Bedeutung gewonnen haben. Die Frage, ob sich solch ein System auch für die Herstellung von Arzneimitteln eignet und welche Kapazitätssteigerung diese neue Technologie für die Produktion mit sich bringt, weckte den Innovationsgeist eines Roche-Teams. Das definierte Projektziel lautete, mehr Chargen pro Woche zu produzieren, um dadurch die Marktnachfrage zu erfüllen und andere Standorte zu ...