Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Simon V.
In der Rubrik Zeitschriften haben wir 2 Beiträge für Sie gefunden
-
Lieferantenqualifizierung in der Pharmaindustrie
Rubrik: GMP / GLP / GCP
(Treffer aus pharmind, Nr. 04, Seite 480 (2015))
Lieferantenqualifizierung in der Pharmaindustrie / Variabilität in Abhängigkeit von der Art der Lieferanten * Der Beitrag beruht auf einem Vortrag beim Seminar „Lieferanten für Pharma: Qualifizierung und Verträge“ im September 2014 in Wien. · Simon V · Simon Pharma Consult e.U., Garsten (Österreich)
Die Anforderungen an der Lieferantenqualifizierung auf Basis des Kap. 7 des EU-GMP-Leitfadens, mit der Anwendung auf alle auszulagernden Tätigkeiten, finden eine konsequente Umsetzung im neuen Kap. 5, das im März 2015 in Kraft tritt. Bei der Anpassung der Systeme für die Lieferantenqualifizierung muss darauf geachtet werden, dass dies nicht zu einer Steigerung des Aufwands und der Kosten für die notwendigen Abläufe führt. Demgegenüber muss aber sichergestellt werden, dass eine GMP-gerechte und qualitativ entsprechende Ausführung der ausgelagerten Tätigkeiten gewährleistet ist, da der pharmazeutische Unternehmer hierfür die Verantwortung trägt.
-
Das neue Site Master File
Rubrik: IT
(Treffer aus TechnoPharm, Nr. 05, Seite 283 (2014))
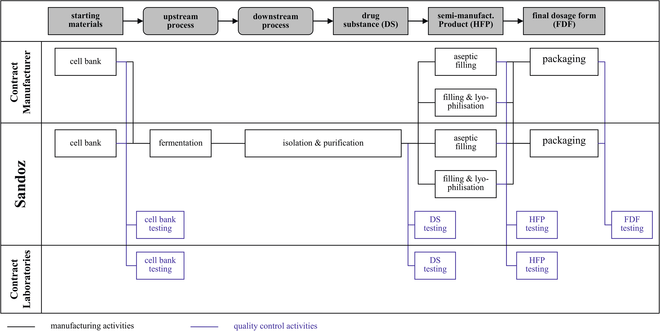
Das neue Site Master File / Beispiel einer praktischen Umsetzung · Haidacher R, Simon V · Sandoz GmbH, Kundl (Österreich) und Simon Pharma Consult e.U., Garsten (Österreich)
Anfang 2011 wurden von der Europäischen Kommission und der Pharmaceutical Inspection Convention / Pharmaceutical Inspection Cooperation Scheme (PIC/S) die endgültigen Dokumente zum Site Master File (SMF) „ Explanatory Notes on the Preparation of a Site Master File“ veröffentlicht [ 1 , 2 ]. Seitdem besteht die Verpflichtung die SMFs gemäß dieser regulatorischen Grundlage (nachfolgend kurz als „ Explanatory Notes“ bezeichnet), die in die EU Guideline Part III [ 3 ] integriert wurden, zu verfassen. Folglich bestand diese Aufgabenstellung auch für den Geschäftsbereich Biopharmaceuticals der Sandoz GmbH am Standort Kundl . Die Erstellung des SMF soll in diesem Beitrag ...