Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12022 Beiträge für Sie gefunden
-

Hocheffiziente Validierung von Sterilisations- und Gefriertrocknungsprozessen
Rubrik: Spektrum
(Treffer aus TechnoPharm, Nr. 01, Seite 55 (2020))
Hocheffiziente Validierung von Sterilisations- und Gefriertrocknungsprozessen / Spektrum
Sterilisations- und Gefriertrocknungsprozesse in der Pharmazie und Medizintechnik unterliegen aufgrund ihres unmittelbaren Einflusses auf die Gesundheit von Menschen strengen Richtlinien, weshalb Unternehmen verpflichtet sind, die spezifikationsgemäße Funktion der Autoklave, Reinigungs- und Desinfektionsgeräte (RDG) oder der Gefriertrocknungsanlagen zu qualifizieren sowie die Prozesse zu validieren. Für diese hochkomplexe Anwendung hat Testo das Datenloggersystem testo 190 entwickelt, das den Anwendern eine einfache und richtlinien-konforme Durchführung ermöglicht. Die Datenlogger testo 190 machen besonders durch ihr robustes Design auf sich aufmerksam: Die Messtechnik befindet sich in einem hermetisch verschlossenen Edelstahlgehäuse und die Batterien in einem separaten Gehäuse aus Polyetheretherketon (PEEK). Durch diese innovative Bauart ist ein schneller ... -
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 01, Seite 16 (2020))
Wagner B | Brinz T | Otterbach S
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung / Teil 2*Teil 1 dieses Beitrags ist erschienen in TechnoPharm 9, Nr. 5, 278–285 (2019). · Wagner B, Brinz T, Otterbach S · Bosch Packaging Technology GmbH, Waiblingen
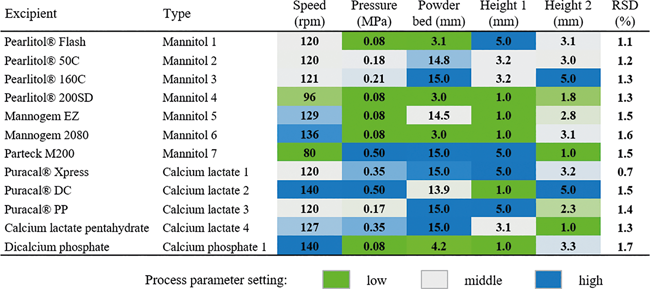
Im ersten Teil dieses Beitrags wurde die Methode der automatisierten Inbetriebnahme (Automated Process Development, APD) vorgestellt. Die automatisierte Inbetriebnahme verwendet statistisch optimierte Versuchspläne und führt diese automatisch, schnell und bei verringertem Pulververbrauch auf dem entsprechenden System oder Anlage durch. Durch die Verwendung der statistischen Versuchsplanung (DoE) sinkt die Anzahl der Versuche gegenüber der klassischen Versuchsplanung. Des Weiteren reduziert sich durch die Automation bzw. die automatisierte Durchführung der Versuche der Aufwand, der notwendig ist, um die Prozessparameter an der Maschine einzustellen. Die kritischen Qualitätsmerkmale (CQA) werden am Ende direkt online oder inline bei der Durchführung der Versuche erfasst. Für die Entwicklung ...
-
Serialisierungssoftware – light, aber effizient
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 01, Seite 22 (2020))
Serialisierungssoftware – light, aber effizient / Framework für eine gesetzeskonforme Serialisierung im Pharmabereich weltweit für den Low-Budget-Bedarf · Höfling J, Pieper T · freier Journalist, München und HED GmbH Haftetikettendruck, Bietigheim-Bissingen
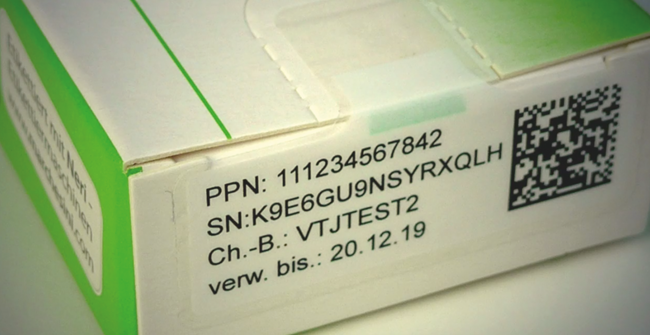
Serialisierung Delegierte Verordnung 2016/161/EU Arzneimittelverpackung Lohnverpacker Lohnhersteller Eine unverwechselbare individuelle Kennzeichnung für Arzneimittelpackungen, die auf Unregelmäßigkeiten und Fälschungen bei einer Packung hinweisen kann, ist mittlerweile weltweit Standard. Die formalen Ausprägungen unterscheiden sich zwar in den einzelnen Weltregionen, das generelle Prinzip ist aber gleich. In der EU und einigen weiteren europäischen Ländern (Schweiz, Norwegen usw.) wird diese individuelle Kennzeichnung (Serialisierung) durch die Fälschungsschutz-Richtlinie 2011/62/EU und die Delegierte Verordnung 2016/161/EU gefordert. Abb. 1 zeigt die Serialisierungsinformationen in „EU-Syntax“. Die Umsetzung der Serialisierung in den Verpackungsprozessen der Pharmazeuten ist sowohl hardware- als auch softwaretechnisch eine komplexe Aufgabe mit umfangreichen Einzelschritten. Es muss sichergestellt werden, ...
-
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 278 (2019))
Wagner B | Brinz T | Otterbach S
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung / Teil 1 · Wagner B, Brinz T, Otterbach S · Bosch Packaging Technology GmbH, Waiblingen
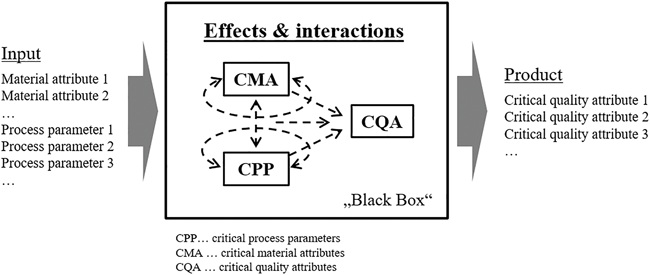
Quality by Design (QbD) Capsule Filling Process Development Design of Experiment (DoE) Powder Filling Ein detailliertes Prozessverständnis ist für die Validierung eines Prozesses unumgänglich. Mit dem Begriff Quality by Design (QbD) setzte die U.S. Food and Drug Administration (FDA) ein Paradigma für die pharmazeutische Prozessentwicklung [1]. Bekannt aus anderen Industrien (etwa Automobil) beschreibt QbD die Idee, dass Qualität nicht erst nachträglich im Produkt getestet wird, sondern bereits bei der Planung und Entwicklung eines Prozesses entsteht. Voraussetzung: Alle entscheidenden Einflüsse auf das Arzneimittel und den Produktionsprozess sowie deren Wechselwirkungen untereinander sind bekannt, und diese können auch gesteuert oder kontrolliert werden. Dann ...
-
Martin Christ Gefriertrocknungsanlagen GmbH
Rubrik: Sonderteil CPhI 2019
(Treffer aus TechnoPharm, Nr. 05, Seite 314 (2019))
Martin Christ Gefriertrocknungsanlagen GmbH / CPhI 2019
Die Martin Christ Gefriertrocknungsanlagen GmbH *) ist ein weltweit führendes Unternehmen in der Entwicklung und Herstellung von Gefriertrocknungssystemen. Ein Schwerpunkt liegt in der Fertigung von Gefriertrocknungsanlagen für pharmazeutische Produkte. Die Anwendungen und die wertvollen Produkte unserer Kunden stehen im Mittelpunkt der Unternehmensausrichtung und sind Motivation, um uns stets neuen technologischen Herausforderungen zu stellen. Ein Beweis dafür ist unser innovatives, vollautomatisches Be- und Entladesystem LyoShuttle, das eine Vielzahl von Vorteilen im Vergleich zu aktuellen Industriestandards bietet. Von einer geringen Anzahl beweglicher Teile im Be- und Entladeprozess bis hin zur einfachen Reinigung und Desinfektion des gesamten LyoShuttle-Systems – höchste Produktqualität und ... -

CPhI 2019
Rubrik: Sonderteil CPhI 2019
(Treffer aus TechnoPharm, Nr. 01, Seite 48 (2020))
CPhI 2019 / Sonderteil CPhI 2019
In eigener Sache An der CPhI worldwide nahmen im Nov. 2019 etwa 49 000 Besucher in Frankfurt/Main teil. Die Messe beherbergt 6 Subevents, die zusammen die komplette Bandbreite der pharmazeutischen Lieferkette abbilden. Das reicht von API´s über den Maschinen- und Anlagenbau bis hin zu Biopharmazeutika und Outsourcing. Bei der 30. Auflage der Leitmesse in Europa organisierte der Editio Cantor Verlag (ECV) erstmals den Gemeinschaftsstand <Excellence in Pharma> ( Abb. 1 ) in der InnoPack-Halle 11.1. Auf diesem stellten die folgenden 9 Mitaussteller ihre Produkte und Dienstleistungen für die Pharmaindustrie vor: chemgineering (GMP Engineering und Beratung) faubel Pharma Services (Labeling) Filtrox (Tiefenfiltration ... -

Pneumatische Automatisierungssysteme
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 01, Seite 57 (2020))
Pneumatische Automatisierungssysteme / Produkte
Die standardisierten Hygienic-Design(HD)-Pneumatik-Schaltschränke Typ 8614 von Bürkert *) erleichtern die Projektierung der Prozesspneumatik inkl. digitaler Eingänge in Hygienic-Anwendungen. Die Systeme sind in 3 standardisierten Baugrößen erhältlich. Modular aufgebaute Ventilinseln mit 8–48 Ventilfunktionen werden mit der AirLINE-Quick-Adaption in Edelstahl direkt im hygienegerechten Schaltschrank montiert und vorverdrahtet, ebenso wie die sonstigen optionalen Baugruppen, z. B. Filterregler, Drucküberwachung, Netzteil oder HD-Wandabstandshalter. Alle vorkonfigurierten Ventilinseln sind standardmäßig mit allen gängigen pneumatischen Prozesssicherheitsmerkmalen und Feldbus-Protokollen ausgestattet. Zudem sind kundenspezifische Ausführungen auf Basis der Standardsysteme problemlos möglich. Da die Baumaße relativ klein sind und alle außenliegenden Teile aus beständigem Edelstahl bestehen, ist das anschlussfertige, geprüfte und zertifizierte HD-Automatisierungssystem sehr ... -
Optimale Luftwechselraten in Reinräumen
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 01, Seite 6 (2020))
Behrens D | Bachhofer J | Zipp B | Keck C | Schäfer J | Runkel F
Optimale Luftwechselraten in Reinräumen / Spannungsfeld zwischen Partikelabreicherung und Wirtschaftlichkeit · Behrens D, Bachhofer J, Zipp B, Keck C, Schäfer J, Runkel F · Behrens Projektmanagement GmbH, Marburg und Technische Hochschule Mittelhessen, Gießen und Philipps-Universität Marburg, Marburg und Justus-Liebig-Universität Gießen, Gießen
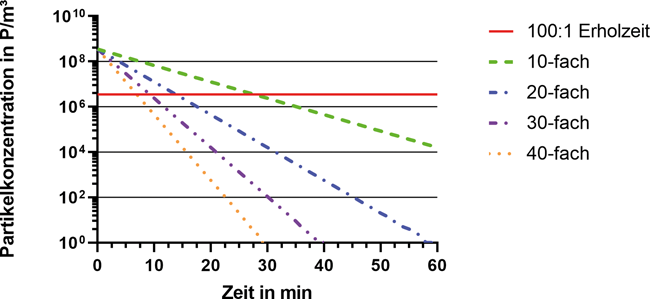
Reinraum Luftwechselrate DIN EN ISO 14644 Clean-up-Phase Erholzeit Die Luftqualität in pharmazeutischen Reinräumen, insbesondere in solchen für die Herstellung steriler Arzneiformen, unterliegt in der pharmazeutischen Industrie den regulatorischen Vorgaben nationaler und internationaler Genehmigungsbehörden [ 1 , 2 , 3 ]. Hierfür geben die behördlichen Richtlinien genaue Grenzwerte für die Konzentration zulässiger Partikel der Größen ≥0,5 μm und ≥5 μm sowie Keime pro m³ Luft vor. Diese Vorgaben können nur durch eine kontinuierliche Zuführung von gefilterter, partikelarmer Luft und eine Abführung partikelbelasteter Raumluft erreicht werden. Damit steht die Luftqualität in direktem Zusammenhang mit der Luftwechselrate des betreffenden Raumes, also dem Wert, wie oft pro ...
-

Pharma Aldenhoven
Rubrik: Sonderteil CPhI 2019
(Treffer aus TechnoPharm, Nr. 05, Seite 314 (2019))
Pharma Aldenhoven / CPhI 2019
Pharma Aldenhoven GmbH & Co. KG *) wurde im Juni 1997 gegründet und ist seither Ihr Lohnhersteller für die richtige Lösung. Als ein marktführender Auftragshersteller sind wir spezialisiert auf die kostengünstige Entwicklung, Herstellung und Konfektionierung nach GMP-Richtlinien in den Kategorien Arzneimittel, Medizinprodukte, Nahrungsergänzungsmittel und Kosmetika. Wir bieten u. a. Nasen-, Ohren- und Rachensprays Bi-Phase-Trinkampullen Salben, Gele, Cremes Säfte, Sirupe, Suspensionen, Tonika, Tropfen Bäder Einreibungen Konfektionierung fester Formen Außerdem bieten wir ein umfangreiches Portfolio an eigenen Zulassungen zum Mitvertrieb, Instrumenteller Analytik (z. B. HPLC, GC, DC, IR) und Stabilitätseinlagerungen nach ICH. Herstellungserlaubnis nach § 13 AMG DIN EN ISO 13485:2016 IFS Food, Version 6.1 (International Food Standard) -

Das GMP-Zertifikat für Anlagenbauer und Maschinenhersteller: Illusorischer Aufwand oder Vorteil für Industrie und Patienten?
Rubrik: Spektrum
(Treffer aus TechnoPharm, Nr. 05, Seite 316 (2019))
Das GMP-Zertifikat für Anlagenbauer und Maschinenhersteller: Illusorischer Aufwand oder Vorteil für Industrie und Patienten? / Spektrum
Die GMP-Belastung für Hersteller und Lieferanten technischer Gewerke wird ständig höher. Genau wie die Pharmaproduzenten sind auch die Anlagen- und Maschinenhersteller den ständig wachsenden Anforderungen diverser GMP-Regelwerke ausgesetzt ( Abb. 1 ). Dabei sind die Forderungen und Erwartungen, die an Techniklieferanten gestellt werden, um als GMP-tauglich zu gelten, meistens nicht exakt standardisiert, sondern risikobasiert definiert – und das durch den Pharmakunden. Das ist zwar legitim und ganz im Sinne einschlägiger Regelwerke (z. B. ICHQ9), erzeugt aber bei den Maschinenlieferanten Uneinheitlichkeit im Ansatz zur Qualitätssicherung gemäß GMP. Und: Pauschale Zertifizierungen mit aktuell am Markt befindlichen non-GMP-Qualitätsstandards reichen den Kunden im Hinblick auf ...
Sie sehen Artikel 701 bis 710 von insgesamt 12022
- Erste Seite
- 69
- 70
- 71
- 72
- 73
- Letzte Seite