CVMP – News | Beitrag aus pharmind 88 | Nr. 5 | Seite XXIV-XXVIII (2026)
11.06.2026Der Wissenschaftliche Ausschuss für Tierarzneimittel (Committee for Veterinary Medicinal Products, CVMP) tagt monatlich bei der Europäischen Arzneimittel-Agentur (European Medicines Agency, EMA) in ...
Haga Bioscience sammelt 2,3 Mio. US-Dollar in Seed-Finanzierungsrunde ein
11.06.2026Haga Bioscience, ein schwedisches Start-up-Unternehmen im Bereich der räumlichen Biologie, gab den Abschluss einer überzeichneten Seed-Finanzierungsrunde in Höhe von 20,9 Millionen SEK (ca. 2,3 ...
Infrastruktur-Zukunftsgesetz: Politische Blockade auflösen
11.06.2026Angesichts der festgefahrenen Verhandlungen über das Infrastruktur-Zukunftsgesetz (IZG) fordert der Verband der Chemischen Industrie (VCI) die Bundesregierung auf, ihren monatelangen Streit ...
Vertex Announces CASGEVY Reimbursement Agreement for the Treatment of Sickle Cell Disease
10.06.2026Vertex Pharmaceuticals Inc. announced that a reimbursement agreement was signed with the GKV-Spitzenverband for its CRISPR/Cas9 gene-edited therapy, CASGEVY® (exagamglogene autotemcel). This ...
meistgelesen
Beitrag aus der Ausgabe 1/2026 der Zeitschrift pharmind
Stabilitätsprüfung von Wirkstoffen und Arzneimitteln
Der Entwurf der neuen ICH-Leitlinie Q1
Stabilitätsuntersuchungen sind ein essenzieller Bestandteil der Arzneimittelentwicklung und -zulassung. Sie dienen dazu, die Qualität, Sicherheit und Wirksamkeit eines Arzneimittels über einen definierten Zeitraum, die Verwendbarkeitsfrist, zu gewährleisten. Die Bedeutung wird auch dadurch verdeutlicht, dass die Stabilitätsleitlinie Q1A „Stability Testing of New Drug Substances and Products“ das erste Thema war, welches im ...

Beitrag aus der Ausgabe 12/2025 der Zeitschrift pharmind
Softwaregestützte Qualitätssicherung
Qualifizierung und Validierung ohne Papier
Der Qualifizierungsprozess ist in der pharmazeutischen Herstellung seit über 30 Jahren etabliert und hat über die Zeit stark an Formalismen und Komplexität der Dokumentation zugenommen [1,2]. Ausgehend von einfachen Checklisten mit Fokus auf technische Aspekte haben sich die Phasen Design Qualification (DQ), Installation Qualification (IQ), Operational Qualification (OQ) und Performance Qualification (PQ) entwickelt. Risikobasierte ...
Beitrag aus der Ausgabe 2/2026 der Zeitschrift pharmind
GDP-Inspektionen
Häufige Mängel bei der Qualifizierung von Logistikdienstleistern und wie man sie vermeidet – Fortsetzung*Vorheriger Teil s. Pharm. Ind. 87, Nr. 11, 1004–1008 (2025).
Die Aufgaben eines Großhändlers nach § 52a AMG sind in der Arzneimittelhandelsverordnung sowie in der EU-GDP-Leitlinie geregelt. Die zuständige Behörde überprüft die Einhaltung dieser Anforderungen im Rahmen von Inspektionen gemäß § 64 AMG.Im Zuge dieser GDP-Inspektionen stellt die Qualifizierung von Logistikdienstleistern einen wesentlichen Prüfpunkt dar. Dieser Aspekt gewinnt insb. dann an Bedeutung, wenn umfangreiche oder ...
Top Themen
Beitrag aus der Ausgabe 5/2026 der Zeitschrift pharmind
Innovationsbooster European Biotech Act
Chancen und Herausforderungen
Der Mitte Dez. 2025 veröffentlichte Vorschlag für einen Biotech Act geht zurück auf eine Kommissionsmitteilung vom März 2024, in der erstmals ein neuer Rechtsrahmen zur Förderung der Biotechnologie für erforderlich gehalten wurde. [1] Kommissionspräsidentin von der Leyen hat diesen Gedanken in ihre im Juli 2024 vorgestellten politischen Leitlinien übernommen und einen Vorschlag für einen Biotech Act angekündigt. Danach soll dieser neue Rechtsakt ...

Vorschau (Änderungen vorbehalten)
Beitrag aus der nächsten Ausgabe 6/2026 der Zeitschrift pharmind
(erscheint am 30.06.2026)
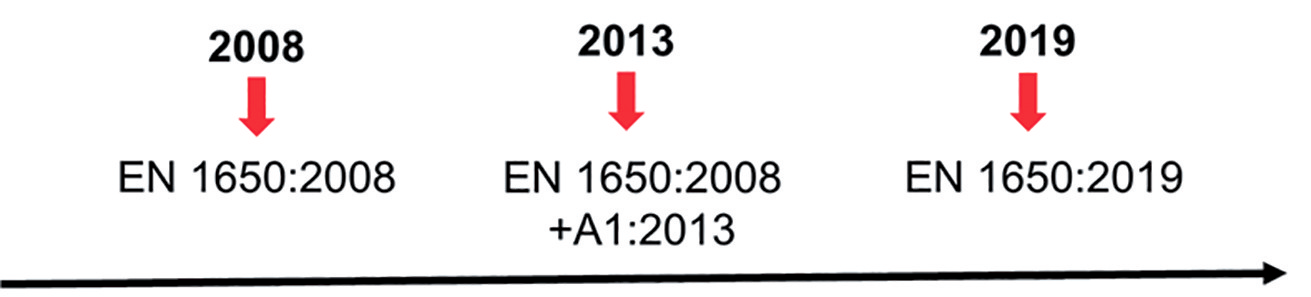
Fungicidal efficacy of alcoholic disinfectants | Impact of cultivation of Aspergillus brasiliensis
To be used as disinfectants in Europe, biocidal products such as alcoholic disinfectants are regulated by the EU’s Biocidal Product Regulation (BPR) EU No. 528/2012. Due to varying lengths of authorization procedures under the BPR, EN (European Norm) methods may change during the evaluation of BPR product authorizations, which may result in different antimicrobial efficacy claims for identical formulations such as 70 % (v/v) propan-2-ol. In this study, we investigated the impact of cultivation of A. brasiliensis established in EN 1650 in 2013 compared to the previous version of EN 1650 on fungicidal efficacy against A. brasiliensis.