Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Denk R.
In der Rubrik Zeitschriften haben wir 14 Beiträge für Sie gefunden
-
Aufbau, Einsatz und Dekontamination von Isolatoren
Rubrik: Technik
(Treffer aus cleanroom & processes, Nr. 03, Seite 142 (2024))
Aufbau, Einsatz und Dekontamination von Isolatoren / Teil 2*Teil 1 dieses Beitrags s. cleanroom & processes 2024;3(2):72–79. · Denk R · SKAN AG, Allschwil
Handschuhe sind die flexible Barriere zwischen dem Raum, in dem sich der Mitarbeiter befindet, und der Zone A im Inneren des Isolators. Durch diese flexible Barriere mit den Handschuhen und Ärmeln, die in der Glasscheibe(n) des Isolators integriert sind, können notwendige Arbeiten innerhalb der Zone A durchgeführt werden ( Abb. 14 ). Sowohl die Handschuhe als auch die Handschuhärmel können jedoch während der Tätigkeit beschädigt werden und dadurch ein Risiko für die Zone A darstellen. Aus diesem Grund wird im Anhang 1 auf Handschuhe an Isolatoren eingegangen. Die Vorgaben des Anhangs 1 sind in Abb. 15 wiedergegeben. Folgende Ursachen für eine Beschädigung der Handschuhe sowie Handschuhärmel sind ...
-
Aufbau, Einsatz und Dekontamination von Isolatoren
Rubrik: Technik
(Treffer aus cleanroom & processes, Nr. 02, Seite 72 (2024))
Aufbau, Einsatz und Dekontamination von Isolatoren / Teil 1 · Denk R · SKAN AG, Allschwil
Barriere-Systeme Annex 1 Handschuhe First-Air Dekontamination Isolatoren kommen in der aseptischen Herstellung in unterschiedlichen Bereichen zum Einsatz. Am häufigsten findet man sie bei der Handhabung von sterilen Produkten. Diese können in flüssiger oder auch fester Form (Feststoff) vorliegen. Auch menschliche oder tierische Zellen werden in neuen Therapien immer häufiger verwendet, z. B. für Zell- und Gen-Therapeutika, die ebenfalls unter aseptischen Bedingungen verarbeitet werden. Nachfolgend werden einige Beispiele für den Einsatz von Isolatoren vorgestellt. Auch wenn menschliche oder tierische Zellen zur Verwendung für neue Therapien aufgrund ihrer Entnahme (meistens in Krankenhäusern) nicht als steril angesehen werden können, besteht auch hier die Anforderung, ...
-
Die Containment-Matrix der ISPE D/A/CH CoP Containment
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 01, Seite 16 (2023))
Schöler M | Nicolai R | Pernau M | Maeck R | Gottlieb O | Hermann F | Maintok M | Denk R | Collins D
Die Containment-Matrix der ISPE D/A/CH CoP Containment / Umgang mit hochaktiven pharmazeutischen Substanzen · Schöler M1, Nicolai R2, Pernau M3, Maeck R4, Gottlieb O5, Hermann F6, Maintok M7, Denk R8, Collins D9 · 1Fette Compacting GmbH, Schwarzenbek 2F. Hoffmann – La Roche AG, Basel 3Bayer AG, Leverkusen 4Boehringer Ingelheim GmbH, Ingelheim 5NNE, Kopenhagen 6Lonza AG, Visp 7Glatt GmbH, Binzen 8Skan AG, Allschwil 9WALDNER Process Systems, Wangen im Allgäu und und
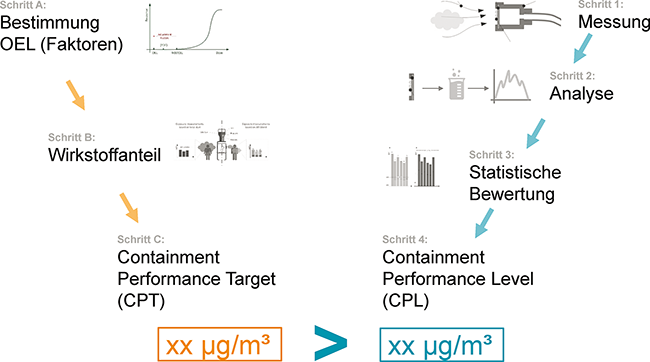
Containment Occupational Exposure Limit (OEL) Arbeitshygiene Rückhalteleistung Hochaktiv SMEPAC Der Schutz von Mitarbeitenden vor dem Kontakt mit gesundheitsgefährdenden Stoffen aus Maschinen und Anlagen durch geeignetes Containment beschäftigt die pharmazeutische Industrie seit vielen Jahrzehnten. Neben der Kenntnis und Nutzung von Containment zum reinen Mitarbeitendenschutz trat in den letzten 10 Jahren v. a. die Notwendigkeit einer übergeordneten Containment-Strategie in den Mittelpunkt, um den Schutz der Patientinnen und Patienten durch die Vermeidung von Kontamination des Produkts und den Schutz der Mitarbeitenden vor Überexposition in Einklang zu bringen. Der erste Leitfaden zum Thema Containment wurde 2005 von der International Society for Pharmaceutical Engineering (ISPE) veröffentlicht [ ...
-
Es gibt 11 weitere Treffer zu Ihrer Anfrage[ Alle Treffer dieser Rubrik anzeigen ]
In der Rubrik Bücher haben wir 1 Buch für Sie gefunden
-
Reinigung und Desinfektion im pharmazeutischen Betrieb
(Treffer aus Büchern)
Vor, während und nach der Produktion – Reinigung und Desinfektion auf höchstem Niveau. Klare, gesicherte Aussagen, wertvolle Hinweise für Problemlösungen und Praxistipps, die Sie bei Ihrer täglichen Arbeit ...