Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Schlögl T.
In der Rubrik Zeitschriften haben wir 2 Beiträge für Sie gefunden
-
Bestimmung der Partikelbelastung von Oberflächen und Equipment in der aseptischen Abfüllung
Rubrik: Originale
(Treffer aus pharmind, Nr. 04, Seite 593 (2016))
Bestimmung der Partikelbelastung von Oberflächen und Equipment in der aseptischen Abfüllung / Schlögl und Schärff • Partikelbelastung in der aseptischen Abfüllung · Schlögl T, Schärff T · Boehringer Ingelheim Pharma GmbH & Co. KG, Biberach/Riß, Germany
Partikelmessung Reinraum Aseptische Abfüllung Messsysteme ISO-Klassifizierung Wischtücher Bei der Abfüllung von Injectabilia unter Reinraumbedingungen ist eine möglichst partikelarme Umgebung gemäß den Klassifizierungen nach ISO 14644-1 nachzuweisen. Behältnisse – z. B. Vials oder Spritzen mit Arzneimitteln zur parenteralen Anwendung, die sichtbare Partikel enthalten – müssen im Zuge einer 100 % visuellen Inspektion aussortiert werden. Je nach Produkt liegt dieser Ausschuss zwischen 0,1–ca. 3,0 % einer Charge. Das Monitoring von in der Luft befindlichen Partikeln ist dabei ein etabliertes Vorgehen für das es bereits standardisierte Messsysteme gibt. Die Kontamination von abgefüllten Einheiten mit Partikeln oder Fasern kann jedoch nicht nur durch luftgetragene Partikel verursacht werden, die Belastung ...
-
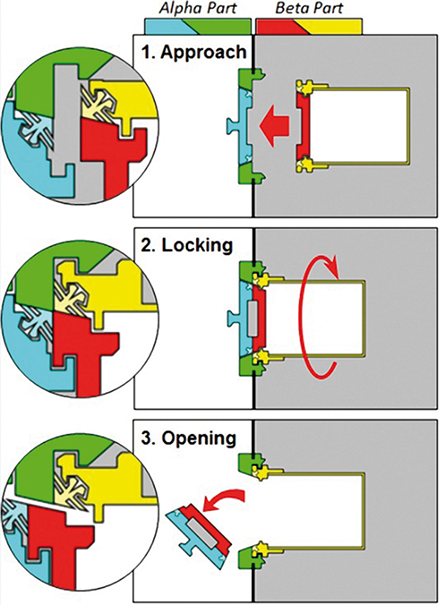
Implementierung der DPTE-Port-Technologie zur Stopfeneinbringung bei einer Vial-Abfüllanlage
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 06, Seite 318 (2015))
Implementierung der DPTE-Port-Technologie zur Stopfeneinbringung bei einer Vial-Abfüllanlage / Schlögl • DPTE-Port-Technologie zur Stopfeneinbringung · Schlögl T · Boehringer Ingelheim Pharma GmbH & Co. KG
Sterilproduktion Stopfenzuführung RABS DPTE port State of the Art Die Anforderungen an aseptisch sichere Prozesse bei der Abfüllung von Injektabilia sind in den letzten Jahren immer weiter gestiegen. Manuelle Prozesse, die früher durch den Nachweis der Beherrschbarkeit im Rahmen von Mediafills bzw. durch das mikrobiologische Monitoring als valide ausgewiesen wurden, werden heute in Audits heftig diskutiert und sind nur noch schwer zu verteidigen. Manuelle Prozessschritte werden daher sukzessive durch technische oder organisatorische Lösungen ersetzt, die eine potenzielle Kontamination durch das ausführende Personal weitgehend ausschließen. Der im folgenden Artikel beschriebene Optimierungsprozess zeigt ein Beispiel für diesen Trend und die Bemühungen, einen ...