In der Rubrik Zeitschriften haben wir 16 Beiträge für Sie gefunden
-
Aktuelle Herausforderungen in der Pharmaproduktion
Rubrik: Editorial
(Treffer aus TechnoPharm, Nr. 02, Seite 57 (2015))
Aktuelle Herausforderungen in der Pharmaproduktion / Editorial
Sehr geehrte Leser des TechnoPharm-Journals, die zweite Ausgabe des TechnoPharm-Journals bringt Ihnen die Fortsetzung unseres Artikels zum Annex 15 „Qualification and validation“, Revision 1 des EU-GMP-Leitfadens. Im zweiten Teil werden die Continuous Process Verification (CPV) und die Ongoing Process Verification (OPV) vorgestellt, deren Bezug zum existierenden Product Quality Report (PQR) aufgezeigt und Voraussetzungen zum Einsatz – wie Quality by Design (QbD) – dargelegt. Der Einsatz von Sicherheitswerkbänken im pharmazeutischen Umfeld ist vielfältig, z. B. Reine Werkbänke für Sterilitätstests, Mikrobiologische Sicherheitswerkbänke oder Zytostatika-Werkbänke. Wir zeigen Ihnen fundiert und übersichtlich die Anforderungen an die verschiedenen Werkbänke auf. Nach der Benutzung müssen u. a. auch ... -
Wenn aus Stunden Tage werden – VPHP-Adsorptions-/Desorptionsverhalten verschiedener Materialien
Rubrik: Reinraum
(Treffer aus TechnoPharm, Nr. 02, Seite 62 (2015))
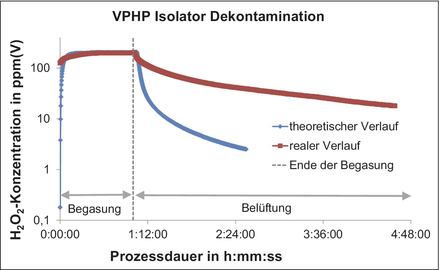
Wenn aus Stunden Tage werden – VPHP-Adsorptions-/Desorptionsverhalten verschiedener Materialien / Adsorption und Desorption von gasförmigem Wasserstoffperoxid (VPHP) verschiedener Materialien im pharmazeutischen Reinraum- und Isolatorbau und dessen Einfluss auf einen Dekontaminationsprozess · Keller M, Weisser S · Fraunhofer IPA, Stuttgart
Gasförmiges Wasserstoffperoxid VPHP Isolator Pharmaproduktion Bio-Dekontamination Adsorption Desorption Aseptische Prozesse in der Pharma-, aber auch in der Lebensmittelindustrie benötigen sterile Umgebungen, damit die notwendige Produktsicherheit gewährleistet werden kann [ 1 ]. Für die Dekontamination von kontrollierten Umgebungsbedingungen stehen verschiedene begasende Verfahren zur Verfügung [ 2 , 3 ] – abhängig von den Eigenschaften des Produkts und der Produktionsumgebung. Eine Variante ist die Dekontamination mit gasförmigem Wasserstoffperoxid (VPHP – vapor phase hydrogen peroxide) [ 4 ]. Hierbei handelt es sich um ein breit etabliertes und anerkanntes Verfahren für eine Dekontamination in Fahrzeugen und Gebäuden, wie etwa Kliniken, und insbesondere in Isolatoren ...
-
GMP-Anforderungen an Werkbänke und Sicherheitswerkbänke
Rubrik: Reinraum
(Treffer aus TechnoPharm, Nr. 02, Seite 70 (2015))
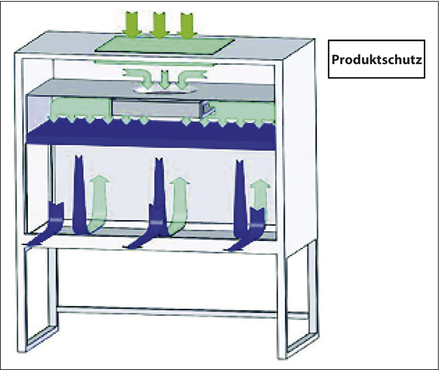
GMP-Anforderungen an Werkbänke und Sicherheitswerkbänke / Nuhn • GMP-Anforderungen an Werkbänke · Nuhn A · GMP-Beratung Nuhn, Niederneisen
Reine Werkbänke Sicherheitswerkbänke Mikrobiologische Sicherheitswerkbänke Produktschutz Personenschutz Zytostatika-Werkbänke Schutzmaßnahmen Reine Räume im pharmazeutischen Betrieb dienen dazu, Produkte vor Kontaminationen zu schützen. In bestimmten Fällen ist es jedoch notwendig, nicht nur das Produkt vor Kontaminationen (hauptsächlich durch Mikroorganismen) zu schützen, sondern auch die Umgebung vor dem Produkt zu schützen. Dazu zählen z. B. Arbeiten mit biologischen Arbeitsstoffen wie auch mit sonstigen reproduktionstoxischen, kanzerogenen und mutagenen Arbeitsstoffen (z. B. Zytostatika, monoklonale Antikörper oder Virustatika). Zu den betroffenen biologischen Arbeitsstoffen zählen Mikroorganismen jeglicher Art, die infektiös oder toxisch sind oder ein allergenes Gefährdungspotenzial für Menschen aufweisen. Um einen Vollschutz für die Mitarbeiter zu vermeiden bzw. ...
-
Die perfekte Kombination: Pulver fördern und dosieren
Rubrik: Technik
(Treffer aus TechnoPharm, Nr. 02, Seite 78 (2015))
Die perfekte Kombination: Pulver fördern und dosieren / Eules • Pulver fördern und dosieren · Eules T · Dec Deutschland GmbH, Geisenfeld
Umfüllen Dosieren Fördern Vakuumförderung Big-Bag-Entleerung niedriger Platzbedarf in Bezug auf die Bauhöhe (keine Falllinie) keine Verstopfungen im Förderschlauch bei schwer fließenden Produkten Erfüllen der Sicherheitsvorschriften und Erreichen eines hohen Containments durch direkt verlinkte Prozessschritte keine Druckschwankungen und deshalb keine Beeinträchtigungen der Wiegegenauigkeit einfache Reinigung im eingebauten Zustand und Ausschluss der Kontaminationsgefahr beim Produktwechsel Das Umfüllen von Pulvern von Großgebinden in Kleingebinde (s. Abb. 1 ) ist eine häufige Aufgabenstellung in der Schüttgutindustrie; eine zentrale Aufgabe dabei ist das Dosieren. In den meisten Fällen werden die Pulver mittels Schwerkraft aus verschiedenen Großgebinden bzw. Schüttgutbehältern entleert. Diese Art der Entleerung erfordert ein Anlagenkonzept ...
-
Mikroorganismen machen Druck
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 02, Seite 84 (2015))
Mikroorganismen machen Druck / Inline-CO2-Messung zur Optimierung biotechnologischer Fermentationsprozesse · Kogej M · Mettler-Toledo GmbH, Gießen
CO 2 -Messung CO 2 -Sensor biotechnologischer Fermentationsprozess Messen des CO 2 -Gehalts Der rasche Fortschritt der Biotechnologie in den letzten Jahren hat bei der Herstellung von Pharmazeutika, Proteinen oder auch Antikörpern zu einer enormen Vielfalt mikrobiologisch hergestellter Produkte geführt. In biotechnologischen Prozessen wird dabei das Wachstum von Mikroorganismen in Bioreaktoren (Fermentern) ausgenutzt, um die gewünschten Stoffe als Nebenprodukt im Zellstoffwechsel herzustellen und in weiteren Schritten zu reinigen. Während des aeroben mikrobiologischen Zellwachstums werden im Stoffwechsel Kohlenhydrate zu Kohlenstoffdioxid (CO 2 ) und Wasser unter Verbrauch von Sauerstoff (O 2 ) „veratmet“. Die Wachstumsphasen der Zellen (Biomasse) richten sich nach ...
-
Risikobasierte Qualifizierung von Lagerbereichen und Transportsystemen
Rubrik: Logistik
(Treffer aus TechnoPharm, Nr. 02, Seite 88 (2015))
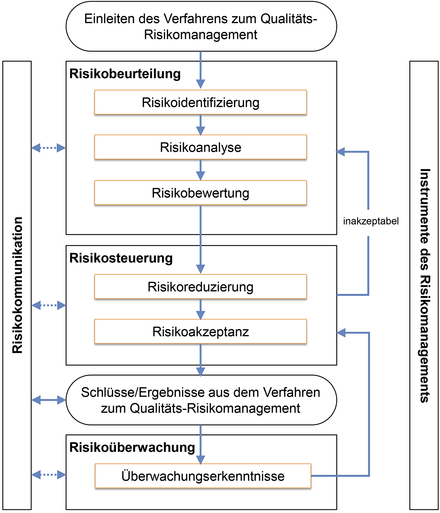
Risikobasierte Qualifizierung von Lagerbereichen und Transportsystemen / Teil 1: Risikomanagement als Werkzeug der Qualitätslenkung optimal nutzen · Salemink N · Testo Industrial Services GmbH, Kirchzarten
Risikomanagement FMEA Lager Transport Qualifizierung GSP GDP Seit dem Inkrafttreten der GDP-Leitlinie [ 1 ] im November 2013 ist bereits etwas Zeit vergangen. Dennoch herrscht zwischen den unterschiedlichen Parteien entlang der Transportkette nicht immer ein einheitliches Verständnis über die Ausprägung und Detailtiefe von qualitätssichernden Maßnahmen wie Qualifizierung und Validierung. Vor allem das Thema Risikomanagement ist in den Bereichen Lagerung und Transport oftmals nicht konsequent im Qualitätssystem integriert und wird stellenweise noch nicht als notwendige und hilfreiche Fehlerpräventionsmaßnahme angesehen. Ziel des vorliegenden Beitrags ist es, eine ganzheitliche Orientierung für die Umsetzung von risikobasierten Qualifizierungsmaßnahmen für Lagerung und Transport zu liefern und ...
-
Soziale Kompetenz – Ingenieure im GMP-Umfeld
Rubrik: Pharmakontext
(Treffer aus TechnoPharm, Nr. 02, Seite 98 (2015))
Soziale Kompetenz – Ingenieure im GMP-Umfeld / Ingenieure haben es auf der emotionalen Ebene schwerer aufgrund ihrer grundsätzlichen Ausrichtung zu logischer Betrachtungsweise · Bergauer R · PP PHARMA PLANING, Freiburg
Ingenieure in GMP FDA-Compliance Soziale Kompetenz GMP und Innovation Führung der Mitarbeiter in Projekten Projektmanagement Ingenieure in GMP FDA-Compliance Soziale Kompetenz GMP und Innovation Führung der Mitarbeiter in Projekten Projektmanagement Was ist das Besondere in der Pharmaindustrie? Es gibt viele GMP-Regeln, die zwingend einzuhalten sind; allerdings sind diese Regeln sehr allgemein formuliert und müssen situativ interpretiert werden. Bei der Interpretation und Umsetzung sind meist mehrere Fachbereiche beteiligt, z. B. Produktion, QA/QC (Quality Assurance/Quality Control), Engineering, Development, Regulatory, Legal, Finanzen. Dadurch ist Vieles von hoher Komplexität und kann nicht mehr allein unter Einbezug der Logik gelöst werden – auch Rücksichtnahme auf die ...
-
Annex 15, Revision 1 – was nun? (Teil 2*Teil 1 des Beitrags ist erschienen in TechnoPharm 2015; 1(6): 40–45.)
Rubrik: GMP-Regularien
(Treffer aus TechnoPharm, Nr. 02, Seite 103 (2015))
Annex 15, Revision 1 – was nun? (Teil 2*Teil 1 des Beitrags ist erschienen in TechnoPharm 2015; 1(6): 40–45.) / Gnibl und Peither • Annex 15, Revision 1 – was nun? · Gnibl R, Peither T · Regierung von Oberfranken, Bayreuth und Maas & Peither AG, GMP-Verlag, Schopfheim
EU-GMP-Leitfaden Anhang/Annex 15 Lebenszyklusmodell Continuous Process Verification (CPV) Quality by Design Design Space Ongoing Process Verification Harmonisierung Prozessvalidierung Der Annex 15 „Qualifizierung und Validierung“ steht für Kontinuität und entwickelt die bestehenden Konzepte der Qualifizierung und Validierung weiter. Die Autoren haben in Ausgabe 1/2015 begonnen, den Annex 15 zu analysieren, und bereits folgende Themen behandelt: 1 Das Lebenszyklusmodell wird der neue Standard. 2 Die URS ist ein Schlüsseldokument in der Qualifizierung. 3 Der traditionelle Validierungsansatz wird präzisiert. 4 Continuous Process Verification ist das Konzept der Zukunft. 5 Ongoing Process Verification ersetzt die Revalidierung. 6 Der Annex 15 harmonisiert auch US-FDA-Anforderungen. Vollständig neu ist im revidierten Annex 15 ...
-
175 Jahre B. Braun Melsungen AG
Rubrik: Spektrum
(Treffer aus TechnoPharm, Nr. 02, Seite 108 (2015))
175 Jahre B. Braun Melsungen AG / Spektrum
Das Jubiläumsjahr der B. Braun Melsungen AG ging vor Kurzem zu Ende. Das Unternehmen feierte im vergangenen Jahr 175-jähriges Bestehen. Am 23. Juni 1839 erwarb Julius Wilhelm Braun die Rosenapotheke in Melsungen und legte damit den Grundstein für den heute weltweit tätigen Konzern mit Niederlassungen in 61 Ländern und 50 000 Mitarbeitern. Die vier Sparten des Gesundheitsversorgers haben ihre Produkte und Dienstleistungen auf unterschiedliche medizinische Felder ausgerichtet: Klinik, Chirurgie, niedergelassener Bereich (Pflege und Arztpraxen) sowie das Segment der extrakorporalen Blutbehandlung. Heute produziert B. Braun mehr als 5 000 Produkte und 120 000 Artikel. Der Konzernjahresumsatz im Jahr 2013 lag bei 5,2 Mrd. Euro. ... -
Bayer HealthCare
Rubrik: Panorama
(Treffer aus TechnoPharm, Nr. 02, Seite 109 (2015))
Bayer HealthCare / Panorama
Werner Baumann, Mitglied des Vorstands der Bayer AG, übernimmt zum April 2015 die Führung des Teilkonzerns Bayer HealthCare. Baumann bleibt Mitglied des Vorstands der Bayer AG sowie des Executive Councils des Unternehmens und behält seine bisherige Verantwortung für die Bereiche Strategie und Portfoliomanagement sowie für die Region Europa bei. Er folgt auf Olivier Brandicourt, Vorsitzender des Vorstands der Bayer HealthCare AG und Mitglied im Executive Council der Bayer AG, der das Unternehmen zum 31.03.2015 verlässt, um neuer CEO bei Sanofi zu werden. Baumann ist seit dem 1. Januar 2010 Mitglied des Vorstands der Bayer AG. Seit dem 1. Oktober 2014 ... -
Merck
Rubrik: Panorama
(Treffer aus TechnoPharm, Nr. 02, Seite 109 (2015))
Merck / pharmind • In Wort und Bild
Andreas Stickler hat die Leitung Controlling des Unternehmensbereichs Healthcare übernommen. Seine bisherige Position als Leiter Mergers & Acquisitions (M&A) übernimmt Roman Morten Werth. In seiner neuen Rolle verantwortet Stickler den zum 1. Jan. 2015 eingeführten Unternehmensbereich Healthcare, der neben dem biopharmazeutischen Geschäft Merck Serono auch die Geschäfte Consumer Health, Biosimilars und Allergopharma umfasst. Stickler ist seit 2002 für Merck tätig, nachdem er zuvor Stationen bei Degussa, Aventis und Hoechst durchlaufen hatte, und war seit 2008 Leiter M&A. Werth arbeitet seit 2008 für Merck und war zuvor mehrere Jahre im M&A-Bereich bei Siemens und Continental AG tätig. -
Pfizer Deutschland
Rubrik: Panorama
(Treffer aus TechnoPharm, Nr. 02, Seite 109 (2015))
Pfizer Deutschland / Panorama
Peter Albiez (49) wird zum 1. März 2015 Vorsitzender der Geschäftsführung der Pfizer Deutschland GmbH. Bereits seit 2009 ist er Mitglied der Geschäftsführung des forschenden Pharmaunternehmens Pfizer in Deutschland und leitet in dieser Funktion seit Anfang 2014 den Geschäftsbereich Global Innovative Pharma. Der studierte Biologe startete seine Karriere bei Pfizer 1996 als Pharmaberater. Er übernahm zunächst Führungspositionen im Vertrieb und Marketing, bevor er 2006 zum Leiter der Vertriebsorganisation aufstieg und 2009 zum Leiter der Geschäftseinheit Primary Care ernannt wurde. Albiez folgt auf Dr. Andreas Penk (49), der den Vorsitz der deutschen Pfizer-Geschäftsführung acht Jahre innehatte und nun zusätzliche Verantwortung im ... -
Pharma-Big Bags
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 110 (2015))
Pharma-Big Bags / Produkte
Kunden aus dem Bereich Pharma vertrauen EMPAC *) bei Behältern zum Verpacken von pharmazeutischen Rohstoffen bis hin zu fertigen APIs (Active Pharmaceutical Ingredients). Pharma-Big Bags von EMPAC sind elektrostatisch ableitfähig verfügbar (gemäß IEC 61340-12 4-4) und mit PE-Folien und Aluminiumverbund-Folien (als Hochbarrierefolie) lieferbar. Möglich ist auch eine Zulassung für den Transport von gefährlichen Gütern. Diese Folien werden unter Einsatz spezieller pharmazeutisch zugelassener Rohstoffe hergestellt, die jeweils mit den Kunden abgestimmt werden. Die Rohstoffe erfüllen dabei folgende Kriterien: lebensmittelunbedenklich nach 10/2011/EG (PIM) und FDA 21 CFR 177.1520 berücksichtigen die europäische Pharmakopöe 3.1.3 und 3.1.4 sowie die US-Pharmakopöe <88> Class VI ... -
Feuchtekalibrierung
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 110 (2015))
Feuchtekalibrierung / Produkte
Mit dem Huminator II hat Testo Industrial Services *) die zweite Generation des Feuchtekalibrators auf den Markt gebracht. Durch die integrierte Temperaturregelung werden mithilfe eines Peltier-Elements (Wärmetauscher) Temperaturen im Bereich von 5 °C bis 50 °C erzeugt. Das leistungsstarke Befeuchtersystem generiert innerhalb kurzer Zeit eine relative Feuchte im Bereich von 5 bis 95 %rF. So beträgt bei einem Angleich der Feuchte von 35 auf 80 %rF die Stabilisierungszeit nur drei Minuten. Eine weit gehende Automatisierung der Kalibrierungen wird durch die zeitliche Programmierfunktion ermöglicht. Das große Touch-Display ermöglicht eine intuitive Nutzung und visualisiert tabellarische und grafische Auswertungen von Messdaten. Der in der Messkammer integrierte, ... -
Anwendungshilfen für Augentropfen
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 110 (2015))
Anwendungshilfen für Augentropfen / Produkte
Gerresheimer *) bietet mit DropAid eine Anwendungshilfe für Augentropfen. Die Anwendungshilfe DropAid ist denkbar einfach und daher auch ganz besonders für Senioren und Kinder geeignet. Sie hilft beim Öffnen der Augentropferflasche mit ihrer kreisrunden Öffnung, die in Form und Größe genau auf deren Verschluss passt. So kann man auch ohne viel Kraft oder Druck die Flasche öffnen. Setzt man DropAid senkrecht mit der halbrunden Öffnung an den Flaschenhals der geöffneten Flasche, kann man diese damit am Auge stabil platzieren, um sich die Tropfen in der richtigen Anzahl verabreichen zu können. DropAid passt zu allen bestehenden "Tropfflaschen - System A" ... -
Kugelhähne
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 02, Seite 110 (2015))
Kugelhähne / Produkte
Bormann & Neupert *) bietet Kugelhähne mit metallischer Sitzdichtung – bestens geeignet, wenn aggressive Medien auf hohe Temperaturen und große Druckdifferenzen treffen. Die Standardausführungen dieser Kugelhähne sind bei Temperaturen bis 350 °C einsetzbar; sie verfügen über hartverchromte Kugeln mit stellitierten Kugelsitzen. Für Hochtemperaturanwendungen bis 500 °C – etwa die Steuerung von Heißdampf – werden wolframcarbid- oder chromcarbidbeschichtete Armaturen geliefert. Die DIN- oder ANSI-gemäßen Normbaulängen und Flanschanschlüsse der Gehäuse aus Kohlenstoffstahl, Edelstahl oder anderen hoch legierten Stählen sichern die passgenaue Integration in neue und bestehende Anlagen. Standardmäßig umfasst das Portfolio die Durchmesser DN 15 bis DN 300 bzw. 0,5 bis 12 Zoll. ...