Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12078 Beiträge für Sie gefunden
-
Erst inspizieren, dann injizieren
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 02, Seite 54 (2023))
Erst inspizieren, dann injizieren / Durchgängige Primärpackmittel-Inspektion im Abfüll- und Verpackungsprozess von parenteralen Arzneimitteln · Wagner H · Heuft Systemtechnik GmbH, Burgbrohl
Primärpackmittel Parenteralia Qualitätsinspektion Integritätsprüfung Arzneimittelsicherheit Nicht nur Injektionszubereitungen müssen unbelastet, hochrein und absolut sicher sein, sondern auch die Primärpackmittel, aus denen sie parenteral – meist intramuskulär oder subkutan – verabreicht werden. Mit innovativen Technologien zur Inline-Inspektion von Vials, die mit klaren Flüssigpräparaten, nach dem Aufschütteln milchig werdenden Suspensionen oder komplett undurchsichtigen Lyophilisaten befüllt sind, lässt sich die Integrität jeder einzelnen Verpackung überprüfen und eine Kontamination des fertigen Produkts wirksam verhindern. Dasselbe gilt u. a. für Blow-Fill-Seal-Behälter und Fertigspritzen. Das Risiko, dass eine von Cracks, Rissen und Leckagen betroffene, möglicherweise undichte und mikrobiologisch verunreinigte Primärverpackung in den Verkehr gerät, wird durch die ...
-
Barriere-Technologie im Lichte des neuen Annex 1
Rubrik: Reinraum
(Treffer aus TechnoPharm, Nr. 02, Seite 80 (2023))
Barriere-Technologie im Lichte des neuen Annex 1 / Teil 1 · Rauschnabel J · Syntegon Technology GmbH, Waiblingen
Barriere-Systeme Isolator RABS Annex 1 Handschuhe 13 Jahre nach Inkrafttreten des Annex 1 „Manufacture of Sterile Medicinal Products“ der Good-Manufacturing-Practice(GMP)-Richtlinie der EU ist am 25.08.2022 eine vollständig überarbeitete Version veröffentlicht worden. Im Umfang um den Faktor 3 gewachsen, stellt der neue Annex 1 (2022) [1] – im Folgenden als „Annex NEU“ bezeichnet – nicht nur wesentlich mehr Details zur Durchführung der sterilen Herstellung bereit, sondern öffnet auch mit der Einführung des Quality Risk Management (QRM) und der Contamination Control Strategy (CCS) regulatorisch den Raum für produktspezifische, im Einzelfall möglicherweise von den Empfehlungen der Richtlinie auch mal abweichende Lösungen. Bei allen Widersprüchen – insbesondere durch ...
-
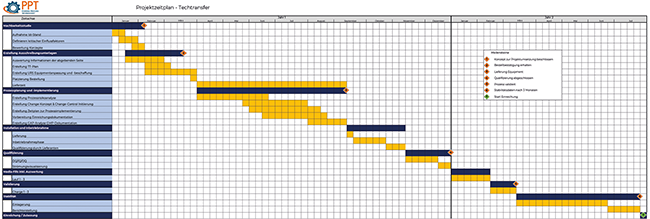
Technologietransfer in der pharmazeutischen Industrie
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 04, Seite 164 (2023))
Technologietransfer in der pharmazeutischen Industrie / Eine Fallstudie · Bieler , Hahn · PPT Pharma Process Technology GmbH, Frankfurt am Main
Technologietransfer Parenteralia Bulklösung Aseptisch Strömungsvisualisierung Wie wird im heutigen globalen Weltmarkt eine Versorgung mit den notwendigen Arzneimitteln zu jeder Zeit sichergestellt? Spätestens im Rahmen der Corona-Pandemie hat sich gezeigt, dass der Zugriff auf lebensnotwendige Arzneimittel durch eine zentralisierte Fertigung zu Lieferengpässen führen kann. Der Technologietransfer von pharmazeutischen Produkten und Herstellprozessen an andere Produktionsorte ist eine zeit- und kostensparende Variante der Kapazitätserweiterung. Es werden vorhandene Kapazitäten genutzt, eine umfangreiche Neubauplanung und das entsprechende Genehmigungsverfahren kann entfallen. Doch was ist im Rahmen eines Technologietransfers von Parenteralia zu beachten? Werden am Ende wirklich Zeit und Kosten gespart? Welche gesetzlichen Vorgaben sind einzuhalten? Die ...
-

Fertigspritzeninspektionslösungen
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 05, Seite 281 (2022))
Fertigspritzeninspektionslösungen / Produkte
Mit weiterentwickeltem gepulsten Röntgen findet der HEUFT *) Syringer einfach mehr bei der Inspektion vorfüllbarer Spritzen. Bei unerreicht niedriger Strahlung identifiziert die lifetime-optimierte, gepulste Röntgeninspektion von der Injektionsnadel durchstochene Soft- und Rigid-Needle-Shields (SNS/RNS), verbogene und deformierte Kanülen oder auch defekte, fehlerhaft montierte, nicht sichere Luer-Lock-Schraubadapter und Originalitätsverschlüsse von Einmalspritzen. Außerdem gelingt so die präzise Überprüfung des korrekten Zusammenbaus der Fertigspritzen. Um damit auch mikrometerkleine Verformungen an der Kanülenspitze (sog. Needle Hooks) sicher zu erkennen, ist schon bald eine innovative Zusatzoptik integrierbar, welche das gepulste Röntgen optimal ergänzt: Noch bevor die Schutzhauben aufgesetzt werden, untersucht eine intelligente Kamera die Nadelspitzen ... -

Bildverarbeitungslösungen
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 05, Seite 278 (2022))
Bildverarbeitungslösungen / Produkte
Mit der innovativen Bildverarbeitungslösung Multi Color Image Processing (MCIP) rückt HEUFT *) zu inspizierende Produkte und Pharma-Primärpackmittel ressourcenschonend ins rechte Licht, um kritische Fremdpartikel, Verunreinigungen, Produktfehler und Verpackungsdefekte noch klarer herauszuarbeiten und von harmlosen Objekten zu unterscheiden. Ursprünglich zur hundertprozentigen Rundum-Inspektion und Integritätsprüfung befüllter Blow-Fill-Seal-Ampullenstreifen und -Infusionsflaschen entwickelt, stellt das innovative Verfahren seine Erkennungsgenauigkeit schon in verschiedenen Kundenanlagen unter Beweis. Direkt integriert in eine intelligente Kamera verbindet MCIP dazu unterschiedliche Illuminationsprinzipien wie etwa Hell- und Dunkelfeldbeleuchtung im Auf- und Durchlicht an nur einer einzigen Inspektionsstation miteinander. Jede eingesetzte Beleuchtungsart ist dabei in einer jeweils anderen Farbe ausgeführt, sodass ... -

Wägetische
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 05, Seite 281 (2022))
Wägetische / Produkte
Friedrich Sailer *) hat den Sailer Wägetisch aus Edelstahl entwickelt. Dieser reinraumtaugliche Anti-Vibrationstisch aus dem Werkstoff 1.4301 verfügt über eine gebürstete Oberfläche mit Oberflächenrauheit Ra <0,8 μm. Durch seine dicht lasergeschweißte Edelstahl-Tischplatten-Konstruktion mit Füllung aus hochfestem Beton und sein hohes Eigengewicht von 130 kg ist er extrem schwingungsarm. Die Oberplatte ist außerdem zur Unterkonstruktion über 4 Dämpfer aus FDA-konformen Kunststoff schwingungsentkoppelt. Alle für den Tisch eingesetzten Materialien sind ebenso wie die Oberflächenqualität FDA-konform. Dieser Wägetisch gewährleistet die maximale Stabilität einer Waage und reduziert Vibrationen auf ein Minimum. Tests mit einer Hochleistungs-Analysewaage von Mettler Toledo (Modell XPR225DR) haben sowohl unter Reinraum- als auch unter ... -

Lesermeinung
Rubrik: Diskussionsforum
(Treffer aus TechnoPharm, Nr. 05, Seite 269 (2022))
Lesermeinung / Diskussionsforum
Zu dem in der Ausgabe 2/2022 (TechnoPharm 12, Nr. 2, 102–109 (2022)) erschienenen Beitrag „Systembetrachtung des Schleifvorganges bei der Fertigung von Edelstahlkomponenten für sensible Anwendungen“ erreichte uns die nachfolgend vollständig wiedergegebene Stellungnahme von Christoph Odwody, NIROPLAN GmbH, Waidhofen/Thaya (Österreich), und Benedikt Henkel, HENKEL Beiz- und Elektropoliertechnik GmbH u. Co. KG, Neustadt-Glewe. Ein Schlusswort der Autoren findet sich im unmittelbaren Anschluss. Austenitische CrNiMo-Legierungswerkstoffe der Qualitäten 1.4404, 1.4435, 1.4539 haben sich zwischenzeitlich aufgrund günstiger Verarbeitungs- und vorteilhaftem Eigenschaftsverhalten bei optimalen Kostenverhältnissen für die erfolgreiche Herstellung von Anlagen im Pharma- und Biotechnologiebereich als klassische Werkstoffe der Wahl etabliert. Neben technisch optimierten Schweißverfahren werden zum qualifizierten Bau entsprechender ... -

Durchzugsscanner
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 05, Seite 277 (2022))
Durchzugsscanner / Produkte
Als neues Einstiegsprodukt bietet das Proofiler RS-System von EyeC *) die hochwertige EyeC-Inspektion zu einem attraktiven Preis-Leistungs-Verhältnis. Der Durchzugsscanner ist dabei besonders platzsparend und ermöglicht die Qualitätsprüfung Ihrer Druckmuster bis hin zum Großformat auch in engsten Arbeitsumgebungen. Der EyeC Proofiler vergleicht die gescannten Muster digital gegen die freigegebene PDF-Vorlage, inspiziert die Druckqualität und stellt gleichzeitig die Richtigkeit und Vollständigkeit des Inhalts sicher – einfach, schnell, objektiv und reproduzierbar. Die neue Softwareversion 4.2 erweitert zudem die Braille-Inspektion, um die Erkennung von zu hoch geprägten Braille-Punkten. Neu ist auch die Code-Konsistenzprüfung, bei der alle 1-D- und 2-D-Codes des gleichen Typs auf ihre ... -

Monitoring-Software
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 05, Seite 277 (2022))
Monitoring-Software / Produkte
Das Erfolgsprodukt Moni.NET Class C der Firma eurogard *) unterstützt Reinraumbetreiber ihr diskontinuierliches Partikel-Monitoring zu digitalisieren, Datenintegrität zu erhöhen und Prozessabläufe bzgl. Zeit, Qualität, Kosten und Nachhaltigkeit zu optimieren. Mit dem Release von Moni.NET Class C Version 2.0 wurden neue Technologien implementiert und der Fokus auf die Reporterstellung gerichtet. Neben weiteren Anhängen wie Audit Trails lassen sich Grenzwertverletzungen farblich kennzeichnen. Neue Reportarten wie „Ausführungsliste“ oder „Wochen-Statusbericht“ in Kombination mit neuen Benutzerrollen und der elektronischen Unterschrift helfen den operativen Ablauf besser zu strukturieren und zu steuern. Auch wurde die Kommunikation zwischen Software und Partikelzählern verbessert, und für eine non-GMP-Nutzung können Reports ohne Compliance-Beurteilung ... -

Abfüllroboter
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 05, Seite 277 (2022))
Abfüllroboter / Produkte
Stäubli *) präsentiert mit dem neuen TX2-60 Stericlean+ das Flaggschiff der neuen Baureihe Stericlean+. Der TX2-60 Stericlean+ verfügt über ein einzigartiges geschlossenes Hygienedesign mit einem optionalen Hollow Wrist samt aseptischem Werkzeugwechsler. Das hohle Handgelenk erlaubt ein wegweisendes Hygienedesign. Der Werkzeugwechsler erhöht die Flexibilität des Roboters und ermöglicht schnelle Prozesswechsel unter sterilen Bedingungen. Der TX2-60 Stericlean+ Sechsachser kann jeden Schritt einer Standardabfüllanwendung übernehmen und dabei belegen, mit welcher Zuverlässigkeit er eine Reihe von Zusatzaufgaben ausführt. Dazu gehören die Entnahme von Behältern, deren Befüllung sowie das Wiegen und Verschließen – und das alles schnell, präzise und zuverlässig. Der Verzicht auf menschliche ...
Sie sehen Artikel 11541 bis 11550 von insgesamt 12078
- Erste Seite
- 1153
- 1154
- 1155
- 1156
- 1157
- Letzte Seite