Header
Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
Sie suchen in allen Bereichen nach dem Autor Graf A.
In der Rubrik Zeitschriften haben wir 10 Beiträge für Sie gefunden
-
Das neue Medizinal-Cannabisgesetz (MedCanG)
Rubrik: Gesetz und Recht
(Treffer aus pharmind, Nr. 06, Seite 521 (2024))
Das neue Medizinal-Cannabisgesetz (MedCanG) / Inhalte und praktische Implikationen · Graf A · Kanzlei Dr. Fandrich Rechtsanwälte, Bonn
Medizinal-Cannabis MedCanG Betäubungsmittel Entkriminalisierung Erlaubnispflicht Bereits 2017 hat der Gesetzgeber mit dem Gesetz zur Änderung betäubungsmittelrechtlicher und anderer Vorschriften die Verkehrs- und Verschreibungsfähigkeit von Cannabisarzneimitteln durch ärztliche Personen hergestellt und damit dem therapeutischen Nutzen 1) von Cannabis Rechnung getragen. War die Anwendung etwa bei schwerwiegend chronisch erkrankten Schmerzpatienten bis dahin nur über eine Ausnahmegenehmigung 2) durch das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) möglich, wurde die Rechtslage durch eine Änderung der betäubungsmittelrechtlichen Vorgaben so angepasst, dass es einer solchen Ausnahmeerlaubnis nicht mehr bedurfte, vielmehr wurde dem Arzt die Umgangsgewalt als kompetentem Entscheidungsträger übergeben. 3) Damit wurden weitere Cannabisarzneimittel verschreibungsfähig. ...
-
Comparison of Raman and MIR spectroscopy for bioprocess monitoring of mammalian cell cultures
Rubrik: Originale
(Treffer aus pharmind, Nr. 11, Seite 1523 (2021))
Graf A | Neubrand C | Baur D | Kadisch M
Comparison of Raman and MIR spectroscopy for bioprocess monitoring of mammalian cell cultures / Graf et al. • Bioprocess Monitoring · Graf A, Neubrand C, Baur D, Kadisch M · Rentschler Biopharma SE, Laupheim und
CHO cell culture multivariate data analysis (MVDA) process analytical technologies (PAT) raman spectroscopy MIR spectroscopy Quality by Design (QbD) and Process Analytical Technologies (PAT) have been an important topic in the biopharmaceutical industry for some years but have recently witnessed a significant push in implementation in manufacturing [ 1 – 3 ]. While the industry generally has the tendency to be slow in adapting new methodologies, recent technical developments, in combination with the trend towards intensified, high-throughput manufacturing, has helped boosting this quick acceptance in the biopharmaceutical industry. Within the PAT/QbD framework, on-line process monitoring, and control of a design ...
-
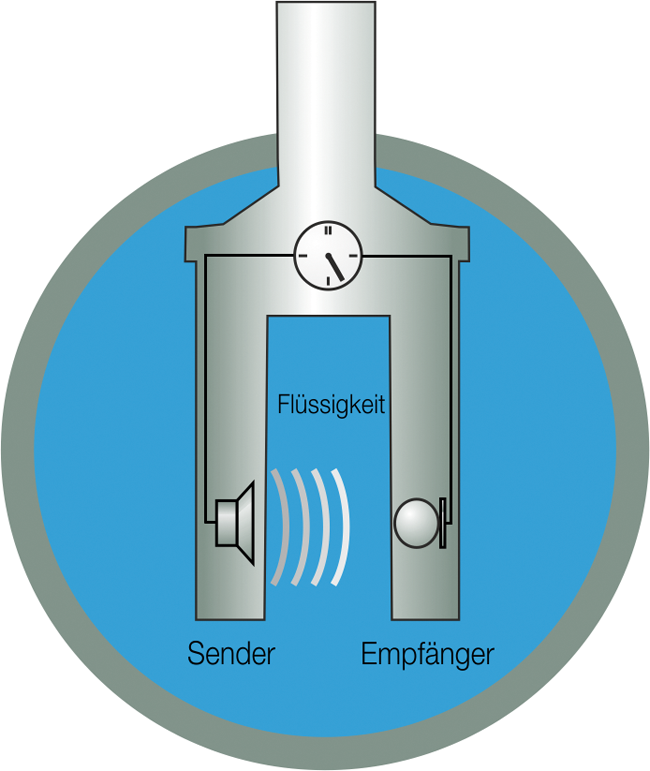
Schallgeschwindigkeitsmesssysteme zur Prozessoptimierung in der Pharmaindustrie
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 03, Seite 166 (2019))
Schallgeschwindigkeitsmesssysteme zur Prozessoptimierung in der Pharmaindustrie / Knape und Graf • Schallgeschwindigkeitsmesssysteme · Graf A, Knape T · SensoTech GmbH, Magdeburg-Barleben
Prozessoptimierung Prozessautomatisierung Konzentrationsüberwachung Qualitätskontrolle wartungsfreie Messung In nahezu allen industriellen Bereichen ist eine Überwachung von Prozessgrößen von großer Bedeutung. Dies ermöglicht die Sicherstellung von Produktqualität und die Vermeidung von Risiken, z. B. Unfällen und Fehlchargen. Oftmals erfolgt diese Kontrolle bei flüssigen Produkten durch die Bestimmung der Konzentration oder Dichte. An die Analysesysteme werden sehr hohe Anforderungen gestellt. Idealerweise erfolgt die Überwachung diverser Messgrößen mit hoher Präzision, um die Fehlerquote zu reduzieren. Zudem ist eine Überwachung in Echtzeit vorteilhaft, da somit Verzögerungen entfallen und sofort eine Reaktion auf Abweichungen im Prozess erfolgen kann. Zudem sind in vielen Produktionsbereichen Probenentnahmen umständlich, zeitintensiv und ...
-
Es gibt 7 weitere Treffer zu Ihrer Anfrage[ Alle Treffer dieser Rubrik anzeigen ]