Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12078 Beiträge für Sie gefunden
-

Track-&-Trace-Kombisysteme
Rubrik: Produktinformationen
(Treffer aus pharmind, Nr. 05, Seite 713 (2018))
Track-&-Trace-Kombisysteme / pharmind • Produktinformationen
Mit dem T2620 stellt Mettler Toledo *) ein kompaktes Kombisystem zur Track-&-Trace-Kennzeichnung von Faltschachteln gemäß der FMD in der EU, des DSCSA in den USA sowie weiterer weltweiter Track-&-Trace-Anforderungen vor. Das Gerät unterstützt hierzu das Aufdrucken variabler Daten – wie Seriennummern, Datamatrix-Codes, Batch-Nummern – sowie statischer Produktkennzeichnungen auf der Faltschachtel. Das Kombisystem überprüft anschließend mittels Kamera die Korrektheit und Druckqualität der Aufdrucke. Dank komfortabler Bedienoberfläche des Terminals zum Aufruf hinterlegter Artikeldaten und der einfach zu handhabenden manuellen Einstellmöglichkeiten kann das System bei Produktwechseln in kürzester Zeit an neue Artikel und deren Faltschachtelabmessungen angepasst werden. Die erstellten Protokolle dienen als ... -

Durchflussmessgeräte
Rubrik: Produktinformationen
(Treffer aus pharmind, Nr. 05, Seite 715 (2018))
Durchflussmessgeräte / pharmind • Produktinformationen
Der Picomag von Endress+Hauser *) kann in alle Rohrleitungen bis 50 mm (2") Durchmesser eingebaut werden. Dafür stehen verschiedene Prozessanschlussadapter zur Verfügung wie NPT-Gewinde, R-Gewinde, Innengewinde, Tri-Clamp oder Victaulic. Das Gerät ist geeignet für Prozesstemperaturen zwischen -10 und +70 °C sowie für Prozessdrücke bis 16 bar. Auf der großen, bedienerfreundlichen Anzeige lassen sich Durchfluss, Temperatur und Summenzähler schnell und einfach ablesen. Mit der Bluetooth-Verbindung sind eine drahtlose Konfiguration oder eine Datenabfrage selbst an schwer zugänglichen Messstellen in bis zu 10 m Entfernung möglich. Das Gerät bietet auch die digitale Datenübertragung zu Prozessleitsystemen mittels IO-Link-Technologie. -

Sterilitätstestisolatoren
Rubrik: Produktinformationen
(Treffer aus pharmind, Nr. 05, Seite 716 (2018))
Sterilitätstestisolatoren / pharmind • Produktinformationen
Metall+Plastic *) stellt den neuen Sterilitätstestisolator Stiso vor. Mehrere Neuerungen zeichnen die Maschine aus: Dazu zählen volle Flexibilität durch den modularen Aufbau, eine schnelle Inbetriebnahme sowie ein im HMI integriertes Handschuhprüfsystem. Mittels katalytischer Belüftung und dem neuen DECOjet®-Verfahren erreicht der Sterilitätstestisolator besonders kurze Zykluszeiten in der Dekontamination. Durch den Einsatz der H 2 O 2 -Flash-Verdampfung ist der Stiso zudem äußerst wartungsarm. Die Maschine ist in Ausführungen für aseptische sowie aseptisch-toxische Anwendungen verfügbar. -

Abfüllgeräte
Rubrik: Produktinformationen
(Treffer aus pharmind, Nr. 05, Seite 714 (2018))
Abfüllgeräte / pharmind • Produktinformationen
Die Watson-Marlow Fluid Technology Group *) präsentiert das neue peristaltische Abfüll-Tischgerät Flexicon PF7. Es ist speziell für den Einsatz unter GMP-Bedingungen, z. B. in der Biotechnologie, Pharmaindustrie oder der Diagnostik ausgelegt. Das Gerät bietet eine zuverlässig wiederholbare Abfüllung von Volumina zwischen 0,2 und 250 ml mit 0,5 % Genauigkeit. Eine intuitive Benutzeroberfläche erleichtert die Validierung und trägt dazu bei, kostspielige Fehler beim Abfüllen hochwertiger Flüssigkeiten zu verhindern. Darüber hinaus bietet das Gerät maximale Flexibilität und eliminiert Kontaminationsrisiken. In Kombination mit den Accusil-Schläuchen wird höchste Präzision beim Dosieren geboten – sowohl nach Masse als auch nach Volumen. In Kombination mit den Flexicon asepticsu Single-Use-Fluid-Path-Lösungen ... -
Evidence of Bellows Sterility in Aseptic Lyophilizers
Rubrik: Analytik
(Treffer aus pharmind, Nr. 05, Seite 686 (2018))
Evidence of Bellows Sterility in Aseptic Lyophilizers / Guttzeit • Bellows Sterility in Aseptic Lyophilizers · Guttzeit M · GEA Lyophil GmbH, Hürth
A lyophilizer or freeze dryer is a quite specific type of equipment within aseptic bio/pharmaceutical manufacturing, mainly because of the complexity of batch-related production. Beyond simple freeze drying, a number of auxiliary processes are also involved. And, depending of the procedural requirements, it may be necessary to include processes such as an inline filter integrity test, a leak test, defrosting, cleaning-in-place (CIP) and/or sterilization-in-place (SIP), all of which have specific design criteria that must be fulfilled: each single process must meet Good Manufacturing Practice (GMP) expectations and ensure the quality of the final product; in addition, any negative impact on ...
-
Neue kLa-Wert-Messung für den optimalen Bioprozess
Rubrik: Biotechnologie
(Treffer aus TechnoPharm, Nr. 05, Seite 300 (2018))
Neue kLa-Wert-Messung für den optimalen Bioprozess / Maischberger und Krainer • kLa-Wert-Messung · Maischberger T, Krainer F · ZETA Biopharma, Lieboch/Graz (Österreich)
PAT Soft-Sensor Sauerstofftransferrate Bioreaktorcharakterisierung Pharmazeutische Produktion Bioreaktordesign ist ein komplexes Thema im Anlagenbau. Die biotechnologische Herstellung von pharmazeutischen Produkten erfolgt überwiegend mithilfe von Mikroorganismen und tierischen Zellkulturen. Damit eine maximale Produktausbeute in diesem System erreicht wird, muss zum einen die Optimierung des Arbeitstiers „Zelle“ auf molekulargenetischer Ebene erfolgen, und zum anderen müssen eben diese Zellen im Bioreaktor optimale Wachstumsbedingungen vorfinden. Eine der wichtigsten Voraussetzung dabei ist eine ausreichende Nährstoff- und v a. Sauerstoffversorgung, damit die Zellatmung optimal ablaufen kann. Weitere wichtige Parameter für die Zellvitalität sind ein effizienter Abtransport von Metaboliten und toxischen Abfallprodukten sowie optimale pH-, Ionen- und Temperaturbedingungen. Neben ...
-

Der Entwurf zum neuen Annex 1
Rubrik: GMP-Expertenforum
(Treffer aus pharmind, Nr. 05, Seite 671 (2018))
Der Entwurf zum neuen Annex 1 / Eine erste Analyse · Brandes R · Hannover
Die mit Spannung erwartete aktualisierte Fassung des Annex 1 zum EU-GMP-Leitfaden wurde im Dezember 2017 zur Konsultation veröffentlicht. Der Projektleiter zur Revision des Annex 1, Andrew Hopkins, versprach auf seinen Seminartouren, dass der neue Anhang detailreicher werden wird. Der Grund dafür ist der immense Wissensverlust durch Ausscheiden von erfahrenen und qualifizierten Mitarbeiter in den letzten Jahren. Diesen Wissensverlust soll der neue Annex 1 kompensieren. Der Entwurf erstreckt sich über 50 Seiten und ist mit vielen neuen Anforderungen und Vorgaben ausgestattet worden. Die neue Gliederung macht die Navigation durch das Dokument einfach und verständlich. Die Bedeutung des neuen Annex 1 besteht darin, dass dieser nicht ...
-

Gefriertrocknung
Rubrik: GMP-Aspekte in der Praxis
(Treffer aus pharmind, Nr. 05, Seite 666 (2018))
Gefriertrocknung / Gieseler • Gefriertrocknung · Gieseler M
Gefriertrocknung wird bei Produkten verwendet, die in Lösung/Dispersion instabil sind und daher nicht als flüssige Arzneiform auf den Markt gebracht werden können. Die Produktlösung wird zunächst eingefroren und nachfolgend das Wasser unter Vakuum durch Sublimation bei niedriger Temperatur entzogen. Da häufig für das Endprodukt Sterilität gefordert wird, jedoch keine Hitzesterilisation möglich ist, muss der Prozess unter aseptischen Bedingungen durchgeführt werden. Das Endprodukt sollte durch ein einheitliches Aussehen und eine schnelle Rekonstitution gekennzeichnet sein.
-

Pseudomonas stutzeri
Rubrik: Analytik / Betriebshygiene
(Treffer aus pharmind, Nr. 05, Seite 682 (2018))
Pseudomonas stutzeri / Ein faltenreiches Bakterium, das aus der Feuchte kommt · Beckmann G · Institut Romeis Bad Kissingen GmbH, Oberthulba
Manche Bakterien erfreuen durch eine ungewöhnliche, makroskopisch sichtbare Morphologie den diagnostizierenden Hygieniker, der sich noch sinnlich-liebevoll seiner Klientel nähert. Dazu zählt auch ein faltenreicher Vertreter aus der Gruppe der Pseudomonaden, der nicht selten anlässlich von mikrobiologischen Umgebungsmonitorings im pharmazeutischen Betrieb isoliert wird: Peudomonas stutzeri . Der Beitrag beleuchtet Vorkommen, klinische Relevanz und Tenazität des typischen Feuchtbereichskeims.
-
Vergleich zweier Double-Pass-RO-Systeme zur PW-Herstellung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 288 (2018))
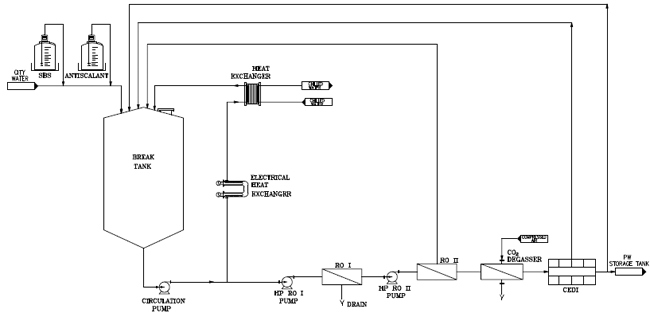
Vergleich zweier Double-Pass-RO-Systeme zur PW-Herstellung / Chemische Vorbehandlung (SBS, AS) versus elektrische Vorbehandlung (ESR, HOD) · Sackstein S · Biopuremax Ltd, Hasdnaot (Israel)
Water for Injection (WFI) Purified Water (PW) Reverse Osmosis (RO) Wassersystem pharmazeutisch Bei dem ersten System (System 1) erfolgt die Vorbehandlung auf der Basis eines Kalkhemmers (antiscalant, AS), um der Abscheidung von Kalk bei der Umkehrosmose vorzubeugen. Außerdem wird Natriumbisulfit (sodium bisulfite, SBS), besser bekannt als Natriummetabisulfat (sodium metabisulfate, SMBS), zur Entfernung von freiem Chlor eingesetzt. Bei dem zweiten System (System 2) basiert die Vorbehandlung auf einer elektrolytischen Kalkreduktion (electrolytical scale reduction, ESR), um der Kalkabscheidung bei der Umkehrosmose vorzubeugen, sowie auf einer hydrodynamischen optischen Entchlorung (hydrodynamic optic de-chlorination, HOD) zur Entfernung von freiem Chlor. Bei beiden Systemen kommen die Double-Pass-Umkehrosmose (double ...
Sie sehen Artikel 3801 bis 3810 von insgesamt 12078
- Erste Seite
- 379
- 380
- 381
- 382
- 383
- Letzte Seite