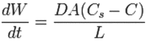Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 11999 Beiträge für Sie gefunden
-

Reinraum Dispergierer
Rubrik: Produktinformationen
(Treffer aus pharmind, Nr. 04, Seite 644 (2014))
Reinraum Dispergierer / pharmind • Produktinformationen
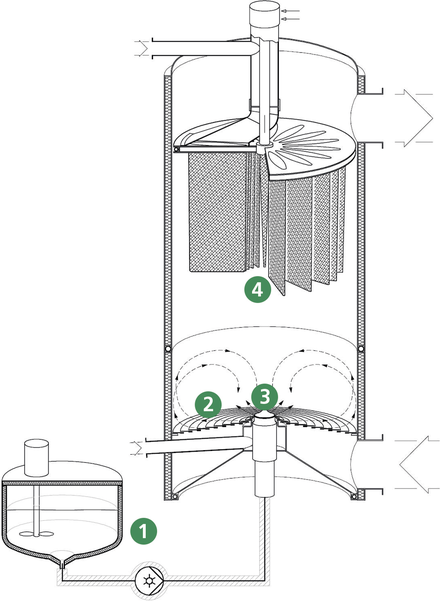
Für die Herstellung von sterilen pharmazeutischen Produkten in Reinräumen bietet die Kinematica AG *) den Reinraum Dispergierer Megatron® MT-SV an. Der Eintrag von Fremdpartikeln ist bei diesem Gerät durch einen vollverkapselten wassergekühlten Hochfrequenz Drehstrommotor ausgeschlossen. Das schlüsselfertige System verfügt über ein Durchsatzvolumen von 1 000 l/h bis 25 000 l/h. Die Lieferung erfolgt mit den in der Pharmazie gewünschten Materialzertifikaten und Protokollen. Ausführungen für Systeme mit Reinraum-Dekontamination stehen auf Anfrage bereit. Das totraumfreie Design ermöglicht durch die SIP/CIP Reinigung eine sehr hohe Hygiene, selbst im Sperrdrucksystem bei Gleitlagerungen sowie bei allen produktberührten Teilen. Der vertikal angeordnete Rotor/Stator (Dispergier-Generator) befindet sich in ... -
Zerkleinern und Mahlen von Tabletten
Rubrik: Verfahrenstechnik
(Treffer aus TechnoPharm, Nr. 05, Seite 238 (2014))
Zerkleinern und Mahlen von Tabletten / Nur die richtige Methode führt zum Erfolg · Benes L · FRITSCH GmbH, Idar-Oberstein;
Die Herstellung von Arzneimitteln unterliegt sehr strengen Richtlinien, und muss daher in Bezug auf Produktqualität höchsten Ansprüchen genügen. Bei der Produktion der unterschiedlichen Wirk- und Hilfsstoffe wird jeder Prozessschritt präzise kontrolliert. Um eine fehlerfreie Analytik zu gewährleisten, muss die Fehlerfortpflanzung direkt im ersten Schritt der Prozesskette unterbunden werden. Der erste Schritt ist dabei immer die Probenaufbereitung. Bei der Tablettenanalytik ist es konkret die Zerkleinerung. Der weitere Erfolg der Analyse ist also direkt abhängig von der Wahl der Methode und den einzustellenden Parametern. [ 1 ] Der Zerkleinerungsprozess gehört zu den Grundoperationen in der Pharmazie. Seit die Menschen ihre ersten Phytopharmaka ...
-
Serie: Sauberkeit und Reinigung in der Produktion
Rubrik: Verfahrenstechnik
(Treffer aus TechnoPharm, Nr. 05, Seite 242 (2014))
Kock H | Holz P | Sternberger-Rützel E
Serie: Sauberkeit und Reinigung in der Produktion / Teil 3: Sauberkeitsprüfung von Maschinen und Anlagen – Equipment und Verfahren · Kock H, Holz P, Sternberger-Rützel E · Fraunhofer-Institut für Physikalische Messtechnik IPM, Freiburg und Harro Höfliger Verpackungsmaschinen GmbH, Allmersbach i.T.
In vielen Produktionsprozessen ist die Sauberkeit von Maschinen und Anlagen ein wichtiges Thema. Mögliche Rückstände sind entweder bereits vor dem eigentlichen Prozess auf der Anlage vorhanden, oder die Rückstände entstehen direkt während der Produktion. Typische Verunreinigungen sind nach der Reinigung verbliebene Rückstände der zu entfernenden Substanzen sowie Rückstände des eingesetzten Reinigungsmittels. Besonders störend sind mikrobiologische Verunreinigungen durch Endotoxine oder Keime und Schimmelpilze. Im Folgenden werden unterschiedliche Verfahren mit und ohne Probenahme vorgestellt. Bevor ein Verfahren zur Reinigungsvalidierung eingesetzt werden kann, muss die verwendete analytische Methode validiert werden. Dabei sind im Wesentlichen drei Punkte zu beachten: die Spezifität, die Empfindlichkeit und ...
-
Kontinuierliches Regelgütemanagement in der Prozessindustrie
Rubrik: Verfahrenstechnik
(Treffer aus TechnoPharm, Nr. 05, Seite 252 (2014))
Kontinuierliches Regelgütemanagement in der Prozessindustrie / Herausforderungen und Erfahrungen aus Anwendersicht · Wolff F · BASF SE, Ludwigshafen
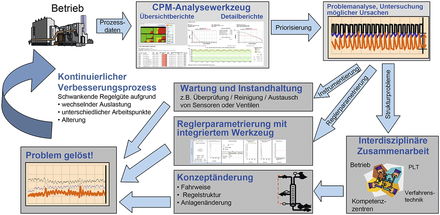
Ein effizienter Anlagenbetrieb in der Prozessindustrie erfordert aufgrund der zunehmenden Volatilität der Märkte und der damit einhergehenden, schwankenden Auslastung eine immer flexiblere Fahrweise. Diese kann dauerhaft nur durch kontinuierliche Optimierungen sichergestellt werden. In diesem Zusammenhang ist auch eine ständige Überprüfung und Anpassung der eingesetzten Regelungen notwendig, um Schwächen wie häufige Handeingriffe oder Oszillationen in bestimmten Betriebsbereichen zu erkennen und zu verringern. Typische Verbesserungsmaßnahmen reichen dabei von einfachem Reglertuning über die Einführung erweiterter Regelkreisstrukturen (z. B. Kaskadenregelungen) bis zu Instandhaltungsmaßnahmen an Ventilen oder dem Tausch unpassend dimensionierter Stellgeräte. Eine Anlage in der Prozessindustrie verfügt je nach Größe und Komplexität über mehrere hundert ...
-
Hot Melt Coating for Controlling the Stability, Release Properties and Taste of Solid Oral Dosage Forms
Rubrik: Verfahrenstechnik
(Treffer aus TechnoPharm, Nr. 05, Seite 258 (2014))
Hot Melt Coating for Controlling the Stability, Release Properties and Taste of Solid Oral Dosage Forms / Haack und Koeberle – Hot Melt Coating · Haack D, Koeberle M · Hermes Arzneimittel GmbH – Division HERMES PHARMA, Pullach und Hermes Arzneimittel GmbH – Division HERMES PHARMA, Pullach
Pharmaceuticals and food supplements are often administered via the oral route, as it is the cheapest, simplest and safest approach available. However, many APIs must be effectively coated during the formulation process in order to successfully exert its functional effects after swallowing. There can be several reasons for this. For instance, many APIs are sensitive to environmental factors such as oxygen, light and humidity, the likes of which can lead to degradation. The internal microenvironment within the dosage form can also be important, with acidic, alkaline or functional excipients often causing API instability. Solid oral dosage forms must also display ...
-
Case Study
Rubrik: Verfahrenstechnik
(Treffer aus TechnoPharm, Nr. 05, Seite 264 (2014))
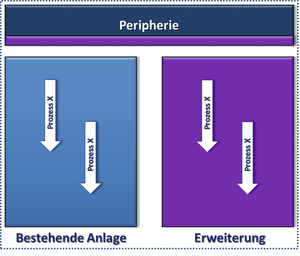
Case Study / Simulation zur Erweiterung und Optimierung einer bestehenden Produktionsanlage · Hutter I, Gienow M · pixon engineering AG, Visp (Schweiz) und pixon engineering GmbH, Mannheim
Die Entwicklung von Computer-Aided-Process-Design (CAPD, Computer-gestützte-Prozess-Entwicklung) begann in der Öl und Gas Industrie bereits in den 1960ern. Dort werden diese Tools seither zur Beschleunigung der Entwicklung und zur Verbesserung von Prozessdesigns verwendet. Heute sind auf dem Markt zahlreiche Simulations-Tools zur Modellierung von chemischen Prozessen erhältlich. Unter anderem sind dies Aspen Plus, ChemCAD, HYSYS, ProSim, PRO/II, etc. Diese Tools wurden v. a. entwickelt, um die in der chemischen Industrie üblichen kontinuierlichen Prozesse zu modellieren. Ähnliche Tools wurden auch für biotechnologische und pharmazeutische Prozesse entwickelt, z. B. Batch Design Kit, BioSolve, SuperPro Designer, Schedule Pro, etc. Im Gegensatz zu den gängigen chemischen Prozessen, werden ...
-
Waagen und mobile Scanner komfortabel in SAP nutzen
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 05, Seite 272 (2014))
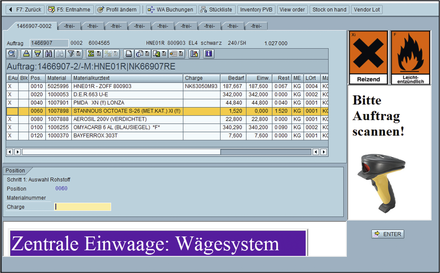
Waagen und mobile Scanner komfortabel in SAP nutzen / Prozessindustrie profitiert von GMP- und 21 CFR Part 11-konformen Lösungen durch optimierte Produktion, Compliance und Kosteneinsparungen · Schroers I · Fujitsu TDS GmbH, Neckarsulm
Um die Herstellung nach Good Manufacturing Practice (GMP) zu gewährleisten, müssen Unternehmen der Pharmabranche entlang der gesamten Prozesskette strenge Richtlinien zur Qualitätssicherung der Produktionsabläufe und -umgebung einhalten. Dabei spielt die Validierung der IT-Systeme, die bei der Planung, Produktion und Auslieferung zum Einsatz kommen, eine herausragende Rolle. Da aufgrund der steigenden Komplexität der Produktionsverfahren zunehmend computergestützte Systeme verwendet werden, erhöhen sich auch der Validierungs- und der damit verbundene zeitliche und finanzielle Aufwand kontinuierlich. So muss sich jeder einzelne Prozessschritt zu jedem Zeitpunkt genau dokumentieren und nachvollziehen lassen. Dies gilt ebenso für Prozesse, die mit branchenspezifischer Zusatz-Software gesteuert werden, wie etwa die ...
-
IntelliCap
Rubrik: Applikationssysteme
(Treffer aus TechnoPharm, Nr. 05, Seite 276 (2014))
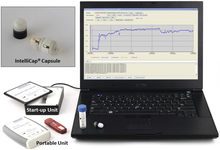
IntelliCap / A pharmaceutical research and development tool for modified release development · Wanke C, Shimizu J · Medimetrics Personalized Drug Delivery B.V., AE Eindhoven, The Netherlands und Medimetrics Personalized Drug Delivery Inc., Briarcliff Manor, NY, USA
Modified Release Drug Absorption Drug Development Drug Device Combination Oral delivery is by far the most convenient and preferred means to administer a medication. Development of an oral product typically starts with an immediate release formulation representing the most frequent and preferred development route. Whenever an oral immediate release formulation does not meet pharmacokinetic (e. g. C max related toxicity), regional delivery (e. g. drug substance is not stable under the acidic conditions in the stomach), or administration frequency requirements (e. g. short half-life), the development of a modified release formulation has to be considered. In addition, developing a modified release formulation may ...
-
Ein sicheres Auge für die Nadel
Rubrik: Applikationssysteme
(Treffer aus TechnoPharm, Nr. 05, Seite 280 (2014))
Ein sicheres Auge für die Nadel / Entwicklungen auf dem Gebiet der Injektionssysteme ermöglichen neue Behandlungsmöglichkeiten und eine verbesserte Compliance für Patienten und Hersteller. · Jakob T · RAUMEDIC AG, Helmbrechts
Mit einem Marktanteil von ca. 25 Prozent erreichten Injektionssysteme im Jahr 2010 den zweiten Platz der meistverkauften Produkte am globalen pharmazeutischen Markt. Übertroffen wurde dies nur noch durch orale Medikamente. Eine zweistellige Zuwachsrate im Bereich der biotechnischen Produkte und einspritzbaren Generika demonstriert den bedeutenden Stellenwert dieses Marktsegmentes. Neben den üblichen vorgefüllten Spritzen, Fläschchen und Behältern werden nun mehr und mehr kundenspezifische und innovative Injektionssysteme, wie Sicherheitsspritzen, speziell angefertigte Pen-Systeme und nadelfreie oder intradermale Injektoren, nachgefragt. Am Markt für injizierbare Medikamente wird ein jährlicher Verbrauch von 2,7 Milliarden vorgefüllten Spritzen verzeichnet. Im Vergleich zu Glassystemen wird in den nächsten Jahren ein zweistelliger ...
-
Das neue Site Master File
Rubrik: IT
(Treffer aus TechnoPharm, Nr. 05, Seite 283 (2014))
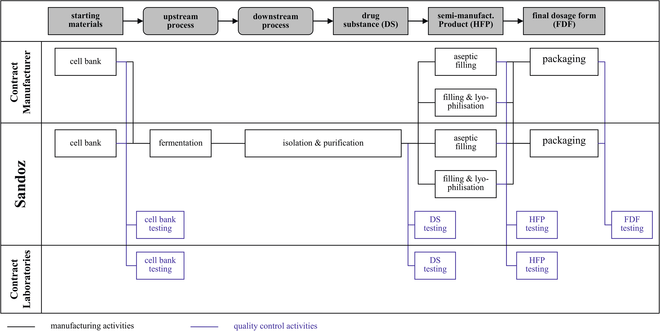
Das neue Site Master File / Beispiel einer praktischen Umsetzung · Haidacher R, Simon V · Sandoz GmbH, Kundl (Österreich) und Simon Pharma Consult e.U., Garsten (Österreich)
Anfang 2011 wurden von der Europäischen Kommission und der Pharmaceutical Inspection Convention / Pharmaceutical Inspection Cooperation Scheme (PIC/S) die endgültigen Dokumente zum Site Master File (SMF) „ Explanatory Notes on the Preparation of a Site Master File“ veröffentlicht [ 1 , 2 ]. Seitdem besteht die Verpflichtung die SMFs gemäß dieser regulatorischen Grundlage (nachfolgend kurz als „ Explanatory Notes“ bezeichnet), die in die EU Guideline Part III [ 3 ] integriert wurden, zu verfassen. Folglich bestand diese Aufgabenstellung auch für den Geschäftsbereich Biopharmaceuticals der Sandoz GmbH am Standort Kundl . Die Erstellung des SMF soll in diesem Beitrag ...
Sie sehen Artikel 5891 bis 5900 von insgesamt 11999
- Erste Seite
- 588
- 589
- 590
- 591
- 592
- Letzte Seite