Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 11999 Beiträge für Sie gefunden
-

Essentials aus dem Pharma- und Sozialrecht
Rubrik: Gesetz und Recht
(Treffer aus pharmind, Nr. 03, Seite 359 (2020))
Essentials aus dem Pharma- und Sozialrecht / Medical Device Regulation – Eine Verordnung mit vielen Herausforderungen · Ehlers A, Kunze S · Ehlers, Ehlers & Partner Rechtsanwaltsgesellschaft mbB, München
Die neue Medizinprodukteverordnung (EU) 2017/745 bringt nicht nur für Medizinproduktehersteller umfassende Änderungen mit sich, die sie zur Einführung von Medizinprodukten auf dem EU-Markt spätestens ab dem 26.05.2020 einzuhalten haben. Obwohl der Gedanke der Patientensicherheit und die länderübergreifende Harmonisierung im Fokus der Verhandlungen standen, ist fraglich, ob nicht gerade die erhöhten Anforderungen an den Herstellungs- und Zertifizierungsprozess die Patientensicherheit in Zukunft gefährden.
-

Aktivitäten des PDCO
Rubrik: europharm
(Treffer aus pharmind, Nr. 03, Seite 352 (2020))
Aktivitäten des PDCO / Throm • PDCO · Throm S · Geschäftsführer Forschung, Entwicklung, Innovation, vfa – Die forschenden Pharma-Unternehmen, Berlin
Bei seiner Sitzung vom 28.–31.01.2020 verabschiedete der Ausschuss für Kinderarzneimittel (PDCO): 12 positive Voten zu pädiatrischen Prüfkonzepten (PIP) für folgende in Entwicklung befindliche Medikamente: Soticlestat zur Behandlung des Chromosom-15q-Duplikationssyndroms und von Cyclin-abhängigen Kinase-ähnlichen 5-Mangelstörungen; Takeda Pharma Baricitinib zur Behandlung des systemischen Lupus erythematodes; Eli Lilly Efgartigimod alfa zur Behandlung der Myasthenia gravis; Argenx Zoliflodacin zur Behandlung von Gonokokken-Infektionen; Entasis Therapeutic allogene, ex vivo expandierte, aus Nabelschnurblut gewonnene hämatopoetische CD34+ Vorläuferzellen/allogene, nicht expandierte, aus Nabelschnurblut gewonnene hämatopoetische reife myeloide und lymphoide Zellen zur Behandlung bei hämatopoetischen Stammzelltransplantationen; Gamida Cell Timrepigen emparvovec zur Behandlung der Chorioderemie; Nightstar Europa autologe CD34+-hämatopoetische Stammzellen, ex vivo ...
-

Aktivitäten des PRAC
Rubrik: europharm
(Treffer aus pharmind, Nr. 03, Seite 354 (2020))
Aktivitäten des PRAC / Aktuelle Empfehlungen des Ausschusses für Risikobewertung im Bereich der Pharmakovigilanz der Europäischen Arzneimittel-Agentur (EMA) · Thurisch B, Sickmüller B · Bundesverband der Pharmazeutischen Industrie (BPI) e. V., Berlin
Der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (Pharmacovigilance Risk Assessment Committee, PRAC) ist in erster Linie für die Beurteilung aller Aspekte des Risikomanagements von Humanarzneimitteln zuständig. Dies umfasst die Ermittlung, Bewertung, Minimierung und Kommunikation der Risiken von Nebenwirkungen, unter gebührender Berücksichtigung des therapeutischen Nutzens des Humanarzneimittels, der Gestaltung und Bewertung der Unbedenklichkeitsstudien nach der Genehmigung sowie Pharmakovigilanz-Audits. Der PRAC gibt somit – abhängig vom jeweiligen Verfahren – Empfehlungen an den Ausschuss für Humanarzneimittel (Committee for Medicinal Products for Human Use, CHMP), die Koordinierungsgruppe (Co-ordination Group for Mutual Recognition an Decentralised Procedures, CMDh), die Europäische Arzneimittelagentur (EMA) oder die Europäische ...
-
Robotics of the future in the pharmaceutical industry
Rubrik: Automation
(Treffer aus TechnoPharm, Nr. 03, Seite 150 (2020))
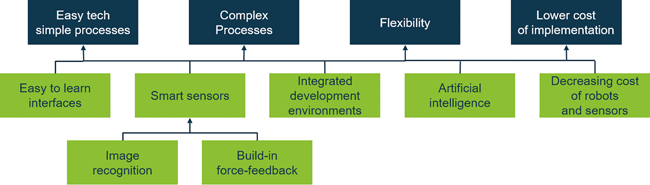
Robotics of the future in the pharmaceutical industry / Coulon • Robotics of the future · Coulon C · INVITE GmbH, Leverkusen
Robotics Pharmaceutical industry Automation Production Laboratory Requirements regarding quality, ergonomics and efficiency reveal the necessity to a much higher degree of automation for the production of pharmaceuticals. In addition, for safety reasons the industry is asked to technically separate humans and high potent substances wherever possible [ 1 , 2 ]. However, looking at production, many activities are currently still carried out by humans, even though there are strong reasons to avoid it. The main message of this article is the hypothesis that modern robotics will provide the pharmaceutical industry with cost-effective and easy-to-use flexible applications as soon as the ...
-

Sterilproduktion
Rubrik: GMP-Aspekte in der Praxis
(Treffer aus pharmind, Nr. 03, Seite 376 (2020))
Sterilproduktion / Prüfung auf Partikel · Brandes R · Wirtschaftsgenossenschaft deutscher Tierärzte eG (WDT), Garbsen
Aus den im Folgenden beschriebenen Verfahren zur Partikelkontrolle muss für jedes Produkt entsprechend den physikalischen Gründen einer elektronischen oder visuellen Erkennung von Partikeln eine optische Kontrollmethode gewählt oder eine Kombination verwendet werden. Weist eine Methode Schwachstellen bei der Erkennung von bestimmten Partikeln auf, müssen diese im Vorfeld der Herstellungsschritte bedacht werden und das Auftreten der betreffenden Fehlerart durch besondere Maßnahmen praktisch ausgeschlossen werden.
-

Digitalisierung der klinischen Forschung – Fluch oder Segen?
Rubrik: Tagungsberichte
(Treffer aus pharmind, Nr. 03, Seite 368 (2020))
Digitalisierung der klinischen Forschung – Fluch oder Segen? / Bericht über das 27. Symposium des Bundesverbands Medizinischer Auftragsinstitute (BVMA) e. V. vom 29.11.2019 in München · Neuer K, Angenendt A · MLM Medical Labs GmbH, Mönchengladbach und Bundesverband Medizinischer Auftragsinstitute (BVMA) e. V., München
Auch 2019 startete das 27. BVMA-Symposium wieder mit dem seit Jahren etablierten und stets gut besuchtem Get-together am Vorabend, bevor der Vorstandsvorsitzende Martin Krauss, zusammen mit Ralf Freese und Dr. Yvonne Rollinger, die alle am selbigen Tag frisch in ihre zweite Amtsperiode starteten, das Symposium im Arabella Sheraton in München eröffnete.
-
Cyber Security by Design in der Anlagenplanung und -realisierung
Rubrik: Automation
(Treffer aus TechnoPharm, Nr. 03, Seite 158 (2020))
Mettler H | Krausz S | Jebari A
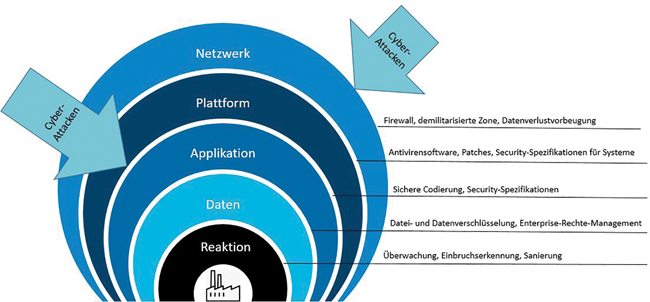
Cyber Security by Design in der Anlagenplanung und -realisierung / Teil 2*Teil 1 dieses Beitrags ist erschienen in TechnoPharm 10, Nr. 2, 108-111 (2020). · Mettler H, Krausz S, Jebari A · Exyte Central Europe, Stuttgart
Die ISO-Normenfamilie 2700X legt die Anforderungen für die Einrichtung, Umsetzung, Aufrechterhaltung und fortlaufende Verbesserung eines Informationssicherheitsmanagementsystems (ISMS) im Kontext der Organisation fest. Außerdem beinhaltet sie Anforderungen für die Beurteilung und Behandlung von Informationssicherheitsrisiken entsprechend der individuellen Bedürfnisse der Organisation. Die Anforderungen sind allgemein gehalten und sollen auf alle Organisationen anwendbar sein, ungeachtet ihrer Art und Größe [ 20 ]. In der Norm ISO 27002 werden konkrete Vorgaben zur Umsetzung genannt. Automatisierte und computerisierte Systeme wurden in den letzten Jahren ein maßgeblicher Bestandteil sowohl in der Bearbeitung als auch in der Speicherung und Archivierung von GMP-relevanten Informationen entlang der Wertschöpfungskette im Unternehmen. Folglich ...
-
Sterilisation flüssiger Produkte in ihren Endbehältnissen
Rubrik: Originale
(Treffer aus pharmind, Nr. 03, Seite 382 (2020))
Sterilisation flüssiger Produkte in ihren Endbehältnissen / Mit dem Dampf-Luft-Gemisch-Verfahren (DLGV) · Möller J · Testo Industrial Services, Kirchzarten
Zugelassene Sterilisationsmethoden verschiedene Sterilisationsverfahren mittels Wasserdampfs Beschreibung der Verfahren mit ihren Vor- und Nachteilen Verfahrensauswahl bei unterschiedlichen Beladungen Nutzung der Letalitätsberechnung als Maß für den Wärmeeintrag Herangehensweise bei einem benötigten homogenen Wärmeeintrag in das Produkt approved sterilization methods various sterilization processes using steam description of the processes regarding their advantages and disadvantages process selection for different loads use of lethality calculation as a measure of heat input approach to a required homogeneous heat input into the product Dampfsterilisationsverfahren Sterilisation flüssiger Produkte Sterilisationszyklen Dampf-Luft-Gemisch-Verfahren DLGV Homogener Wärmeeintrag Sterilisation ist ein wichtiger qualitätsinduzierender Prozessschritt bei der Herstellung von pharmazeutischen Produkten. Gerade bei ...
-
Robotics and Pulsed Light for a New Decontamination Process
Rubrik: Technik
(Treffer aus pharmind, Nr. 03, Seite 392 (2020))
Robotics and Pulsed Light for a New Decontamination Process / Ebeling • Robotics and Pulsed Light · Ebeling M · EbeTech GmbH, Scheeßel (Germany)
The Robotic Tub Decontamination System, born in 2017 from the joint commitment between a highly specialized European manufacturer of complete lines for the aseptic processing and a pioneer of pulsed light in-line packaging decontamination, integrates robotics and pulsed light technology. 2 innovations combined to bring pulsed light technology’s benefits to the pharmaceutical sector. The Robotic Tub Decontamination System (RTDS2) uses pulsed light to decontaminate tubs suitable for pharmaceutical ready-to-use containers. Pulsed light cannot be considered new technology, considering that it is known since the 1980s and it has already been applied to the food industry. Pulsed light is one of many ...
-
Additive Fertigung in der Arzneimittelproduktion
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 03, Seite 164 (2020))
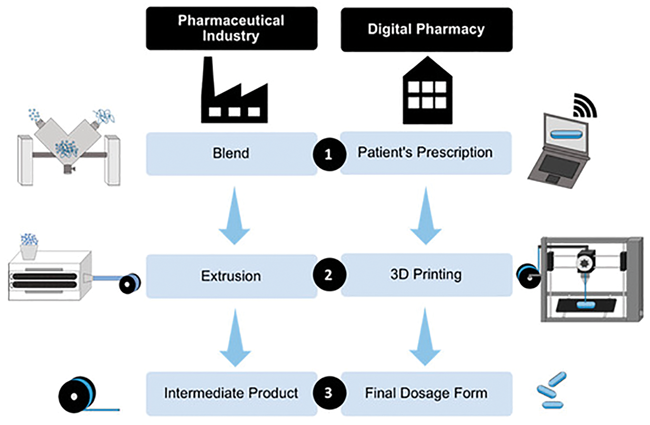
Additive Fertigung in der Arzneimittelproduktion / Potenziale und Herausforderungen · Tidau M, Finke J · Institut für Partikeltechnik (iPAT), Zentrum für Pharmaverfahrenstechnik (PVZ), TU, Braunschweig
3D-Druck Additiver Herstellungsprozess Individualisierung Drucktechnologien 3D-gedruckte Arzneiformen Additive Fertigungsverfahren halten seit vielen Jahren Einzug in die verschiedensten Industriezweige. Dies gilt spätestens seit der Zulassung des von Aprecia Pharmaceuticals LLC. entwickelten 3D-gedruckten Antiepileptikums Spritam ® [ 1 ] durch die U.S. Food and Drug Administration (FDA) im Jahr 2015 auch für die Pharmaindustrie. Weitere Firmen (z. B. FabRx Ltd., Multiply Labs) haben sich der Entwicklung 3D-gedruckter Arzneiformen verschrieben und erste für die additive Fertigung von Arzneimitteln ausgelegte Anlagen (z. B. der AutoCompounder von Vitae Industries Inc. und Anlagen von DiHeSys GmbH) werden vertrieben. Allerdings wurde bislang trotz großem Forschungsaufwand [ 2 , ...
Sie sehen Artikel 9191 bis 9200 von insgesamt 11999
- Erste Seite
- 918
- 919
- 920
- 921
- 922
- Letzte Seite