Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12078 Beiträge für Sie gefunden
-

Aktivitäten des PRAC
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 92 (2017))
Aktivitäten des PRAC / Aktuelle Empfehlungen des Ausschusses für Risikobewertung im Bereich der Pharmakovigilanz der Europäischen Arzneimittelagentur (EMA) Die Aufgaben des PRAC sind im PRAC-Beitrag in Pharm Ind. 2016;78(1):80 beschrieben. · Thurisch B, Sickmüller B · Bundesverband der Pharmazeutischen Industrie (BPI) e. V., Berlin
Folgendes neue Referral-Verfahren wurde gestartet: injizierbare Arzneimittel zur Behandlung allergischer Reaktionen, die Laktose aus Kuhmilch enthalten, Art.-31-Verfahren Das Verfahren für injizierbare Arzneimittel zur Behandlung akuter allergischer Reaktionen, die Laktose aus Kuhmilch enthalten, wurde auf Ersuchen Kroatiens am 1. Dez. 2016 gemäß Art. 31 der Richtlinie 2001/83/EG eingeleitet. Der Review umfasst injizierbare Arzneimittel, die das Corticosteroid Methylprednisolon enthalten und zur Behandlung der Symptome schwerer allergischer Reaktionen eingesetzt werden. Insbesondere umfasst die Überprüfung Arzneimittel, die aus Kuhmilch gewonnene Laktose (Milchzucker) enthalten und folglich Spuren von Kuhmilchproteinen aufweisen können. Diese Arzneimittel sind in nationalen Verfahren zur Verabreichung durch Injektion in eine Vene oder einen Muskel ...
-

Aktivitäten des COMP
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 88 (2017))
Aktivitäten des COMP / Throm • COMP · Throm S · Geschäftsführer Forschung/Entwicklung/Innovation, vfa – Die forschenden Pharma-Unternehmen, Berlin
Vom 6.–8. Dez. 2016 fand bei der europäischen Arzneimittelagentur EMA in London die 184. Sitzung des Ausschusses für Arzneimittel gegen seltene Krankheiten (Committee for Orphan Medicinal Products, COMP) statt. Dabei verabschiedete dieser: 20 Empfehlungen für die Zuerkennung des Status „Arzneimittel gegen eine seltene Krankheit“ für die folgenden, in Entwicklung befindlichen Medikamente: [5,10,15,20-Tetrakis(4-carboxyphenyl)-21H,23H-porphin]manga n(III) chlorid zur Behandlung des Cockayne-Syndroms; Institut Pasteur 5-Aminolävulinsäure zur Behandlung von Gliomen; Centre Hospitalier Universitaire de Lille Hydroxychloroquin zur Behandlung des Antiphospholipid-Syndroms; Centre Hospitalier Universitaire d' Angers Leuprorelin acetat zur Behandlung des ererbten hypogonadotrophen Hypogonadismus; Stichting Centre for Human Drug Research Pioglitazon hydrochlorid zur Behandlung des plötzlichen ...
-

Aktivitäten von CHMP und CMDh
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 80 (2017))
Aktivitäten von CHMP und CMDh / Throm • CHMP und CMDh · Throm S · Geschäftsführer Forschung/Entwicklung/Innovation, vfa – Die forschenden Pharma-Unternehmen, Berlin
Der Ausschuss für Humanarzneimittel (CHMP) erzielte bei seiner Sitzung vom 12.–15. Dez. 2016 bei der europäischen Arzneimittelagentur EMA in London folgende Ergebnisse: Der CHMP verabschiedete: 3 Zulassungsempfehlungen inkl. Pharmakovigilanzplänen für folgende Medikamente mit einem neuen Wirkstoff: Alecensa® (Alectinib) Hartkapseln von Roche zur Behandlung von Patienten mit ALK-positivem, fortgeschrittenem, nicht kleinzelligem Lungenkarzinom, die mit Crizotinib vorbehandelt sind. Der Wirkstoff ist ein Proteinkinasehemmer (L01XE36), der die Autophosphorilierung von ALK und davon abhängigen Signalproteinen und die Vermehrung von ALK-abhängigen Krebszellen hemmt. Der Nutzen von Alecensa liegt in dessen bedeutender Aktivität auf ALK-positive Lungenkrebszellen mit objektiven Ansprechraten von 50,8 % bzw. 52,2 % bei 2 Phase-III-Studien. Die ...
-
Neue Herausforderungen an Ergänzende bilanzierte Diäten durch EFSA-Dossiers
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 75 (2017))
Neue Herausforderungen an Ergänzende bilanzierte Diäten durch EFSA-Dossiers / Teil 1 · Turowski A · Diapharm GmbH & Co. KG, Münster
Seit dem 20. Juli 2016 gilt die EU-Verordnung Nr. 609/2013 über Lebensmittel für Säuglinge und Kleinkinder, Lebensmittel für besondere medizinische Zwecke und Tagesrationen für eine gewichtskontrollierende Ernährung. Dieses Datum bedeutet insoweit einen Meilenstein, als durch diese Verordnung (auch bezeichnet als Speziallebensmittelverordnung oder Foods for Specific Groups [FSG], also Lebensmittel für spezielle Verbrauchergruppen) nach über 30 Jahren das Konzept der Lebensmittel für eine besondere Ernährung (diätetische Lebensmittel) im europäischen Recht aufgegeben wird. In diesem Beitrag wird erläutert, welche Änderungen, Probleme aber auch Chancen sich für die Produktkategorie Lebensmittel für besondere medizinische Zwecke (Food for special medical purposes [FSMP]) und hier besonders für die ...
-

Re-use of Extraction Solvents in the Manufacture of Herbal Extracts
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 71 (2017))
Bauer S | Herde A | Schlegel P | Daniel M | Tegtmeier M | Brand N | Steinhoff B
Re-use of Extraction Solvents in the Manufacture of Herbal Extracts / Bauer et al. • Re-use of Extraction Solvents · Bauer S, Herde A, Schlegel P, Daniel M, Tegtmeier M, Brand N, Steinhoff B · 1Max Zeller Söhne AG, Romanshorn, Schweiz und 2SALUS Haus GmbH & Co. KG, Bruckmühl und 3Dr. Willmar Schwabe GmbH & Co. KG, Karlsruhe und 4Finzelberg GmbH & Co. KG, Andernach und 5Schaper & Brümmer GmbH & Co. KG, Salzgitter und 6Maros Arznei GmbH, Fürth und 7Bundesverband der Arzneimittel-Hersteller e. V. (BAH), Bonn
The majority of herbal preparations used in herbal and traditional herbal medicinal products are herbal extracts. For their production, mainly mixtures of ethanol or methanol and water are used, but also water, acetone or ethyl acetate, etc. In many cases organic solvents are recovered/recycled during the production process for environmental reasons as well as due to safety considerations. Such a procedure is generally accepted but questions on the quality of these recovered/recycled solvents and of the extracts resulting from their use arise. This publication intends to collect experiences of manufacturers from their daily practice and to present recommendations for the ...
-

Qualification of Suppliers of Cultivated and Wild Collected Medicinal Plants
Rubrik: GMP / GLP / GCP
(Treffer aus pharmind, Nr. 01, Seite 66 (2017))
Raiser M | Hofmann W | Stekly G | Tegtmeier M | Torres Londoño P | Steinhoff B
Qualification of Suppliers of Cultivated and Wild Collected Medicinal Plants / Raiser et al. • Qualification of Suppliers · Raiser M, Hofmann W, Stekly G, Tegtmeier M, Torres Londoño P, Steinhoff B · 1Dr. Willmar Schwabe Business Services GmbH & Co. KG, Karlsruhe und 2Biologische Heilmittel Heel GmbH, Baden-Baden und 3SALUS Haus GmbH & Co. KG, Bruckmühl und 4Schaper & Brümmer GmbH & Co. KG, Salzgitter und 5Kräuter Mix GmbH, Abtswind und 6Forschungsvereinigung der Arzneimittel-Hersteller e. V. (FAH), Bonn und 7im Namen der Arbeitsgruppe „Lieferantenqualifizierung“ der Forschungsvereinigung der Arzneimittel-Hersteller e. V. (FAH)
Each manufacturer of medicinal products has to establish a Quality Assurance (QA) system in order to guarantee a high and consistent quality of its products. This also applies to the manufacture of medicinal products of herbal origin (herbal products and homeopathic medicinal products). According to Chapter 5 of the EU Good Manufacturing Practices (GMP) Guideline [ 1 , 2 ], qualification of suppliers is part of the QA system. Suppliers 1) of cultivated and wild collected raw materials of natural origin have to be qualified as well. However, due to the natural origin and the particularities of the production of ...
-

Marketing-Trends
Rubrik: Pharma-Marketing
(Treffer aus pharmind, Nr. 01, Seite 60 (2017))
Marketing-Trends / Teil 1: Content Marketing in Pharma · Umbach G · Healthcare Marketing Dr. Umbach & Partner, Bonn
Content Marketing im Pharma-Bereich bedeutet, hochwertige, relevante Inhalte zu entwickeln und zu vermitteln mit der Absicht, den Zielgruppen das Leben zu erleichtern. Wenn das gelingt, werden sich die Zielgruppen freiwillig auf die Firma zubewegen und sich für deren Produkte oder Services interessieren, sodass diese Zielgruppen leichter als Kunden gewonnen und gebunden werden können.
-
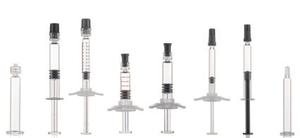
Spritze
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 01, Seite 57 (2017))
Spritze / Produkte
Gerresheimer *) hat die metallfreie 1 ml long Luerlock Gx RTF Spritze zur Serienreife gebracht. Denn insbesondere für auf biotechnologisch hergestellten Wirkstoffen basierende Medikamente benötigen Pharmaproduzenten vorfüllbare Spritzen, bei denen Metallverunreinigungen idealerweise ausgeschlossen sind. Ein Transfer auf weitere Luerlock-Spritzengrößen oder auf Luerkonus-Spritzen verschiedener Größe ist jederzeit möglich. Der für die Konusformung eingesetzte Dorn besteht bei der neuen Technologie nicht mehr aus dem üblicherweise eingesetzten Wolfram oder einem alternativen Metall, sondern aus einer speziellen Keramik. Externe Tests zeigen, dass das neue Verfahren der Konusformung rückstandsfrei arbeitet. Es werden also nicht nur Metallspuren, sondern auch Verunreinigungen durch die verwendete Keramik ausgeschlossen. In ... -

UV-Tinte
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 01, Seite 57 (2017))
UV-Tinte / Produkte
Videojet Technologies *) hat eine innovative fluoreszierende UV-Tinte vorgestellt, mit der sich gestochen scharfe Codes auf hochwertige Pharmaprodukte aufbringen lassen. Die neue Tinte ist bei normalen Lichtverhältnissen farblos und fluoresziert unter Schwarzlicht bläulich. Sie ist MEK-lösungsmittelbasiert und bietet daher gute Haftungseigenschaften auf einer Vielzahl verschiedener Substrate, darunter beschichtete Kartons, glänzende Etiketten, Vialdeckel und -verschlüsse und dunkle Substrate, auf die ein Barcode aufgebracht werden soll. Die farblose UV-Tinte eignet sich ideal für GS1-DataMatrix und andere 2D-Codes und hält auch Autoklavierungen stand. Sie bietet Trocknungszeiten von 2–3 Sekunden auf nicht porösen Substraten wie ABS, HDPE, PET, PVC und Nylon. Die Haftbarkeit ... -

Ventilantrieb
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 01, Seite 57 (2017))
Ventilantrieb / Produkte
Mit dem neuen elektromotorischen Ventilantrieb GEMÜ eSyDrive reagiert die Firma GEMÜ *) auf die steigenden Anforderungen im Bereich elektromotorisch betriebener Ventile. Basierend auf dem Hohlwellenprinzip in Verbindung mit bürsten- und sensorloser Technik setzt GEMÜ eSyDrive Maßstäbe in Bezug auf Kompaktheit, Zuverlässigkeit und Genauigkeit. Zusätzlich bietet der selbsthemmende Antrieb eine hohe Reproduzierbarkeit der Positionierung und ist somit für genaue Regelanwendungen sehr gut geeignet. Die Ethernet-basierende eSy-Web Schnittstelle in Verbindung mit einem integrierten Webserver ermöglicht den Datenaustausch von Parametrier- und Diagnosedaten sowie eine Vernetzung mehrerer Geräte. Nach dem Start der Initialisierung stellt sich der Antrieb automatisch auf das jeweilige Prozessventil ein, ...
Sie sehen Artikel 4671 bis 4680 von insgesamt 12078
- Erste Seite
- 466
- 467
- 468
- 469
- 470
- Letzte Seite





