Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 11999 Beiträge für Sie gefunden
-

Life-Sciences-Standort im Herzen Europas
Rubrik: Statements
(Treffer aus pharmind, Nr. 01, Seite 10 (2026))
Life-Sciences-Standort im Herzen Europas / Wie die Schweiz ihre internationale Führungsrolle behaupten kann · Buholzer R · Interpharma – Verband der forschenden pharmazeutischen Firmen der Schweiz
Die Schweiz gilt seit Jahrzehnten als eine der weltweit führenden Life-Sciences-Nationen. Forschung, Entwicklung und Produktion pharmazeutischer Innovationen sind hier nicht nur Wirtschaftsfaktor, sondern Fundament des Wohlstands. Doch dieses Erfolgsmodell steht zunehmend unter Druck. Politischer Kostendämpfungsdrang, regulatorische Hürden und geopolitische Spannungen gefährden den Produktions- und Forschungsstandort sowie die Versorgungssicherheit. Das Schweizer Gesundheitssystem basiert auf einer obligatorischen Krankenversicherung, die über individuelle Prämien finanziert wird. Das führt zu einer besonderen Dynamik: Steigende Gesundheitsausgaben schlagen direkt auf die Haushalte der Bevölkerung durch. Entsprechend groß ist der politische Druck, Kosten zu begrenzen. In diesem Umfeld muss sich die Pharmaindustrie nicht nur wirtschaftlich behaupten, sondern auch ...
-

Gain-of-Function-Forschung
Rubrik: Exkurs
(Treffer aus pharmind, Nr. 01, Seite 12 (2026))
Gain-of-Function-Forschung / Nutzen und Gefahr · Stoll G
Gentechnologie SARS-CoV-2 Biosicherheit Biowaffen Pandemie Man hätte gewarnt sein können. Im Jahr 2015 veröffentlichte Ralph Baric von der University of North Carolina mit seinem Team eine Publikation, in der sie zeigen konnten, dass ein Sars-CoV-2-ähnliches Virus, das zu der Zeit in chinesischen Fledermaus-Populationen häufig auftrat, nach dem gentechnischen Zusatz der Information für ein Spikeprotein eines anderen Fledermaus-Coronavirus in die Lage versetzt wurde, sowohl Labormäuse wie auch menschliche Zellen zu befallen. Weder Antikörper noch ein damals zur Verfügung stehender Totimpfstoff waren in der Lage, diesen Befall zu unterbinden. „ Unsere Ergebnisse deuten auf ein potenzielles Risiko hin, dass es in Viren, ...
-
Containment in ADC Facilities
Rubrik: Produktion
(Treffer aus cleanroom & processes, Nr. 01, Seite 14 (2026))
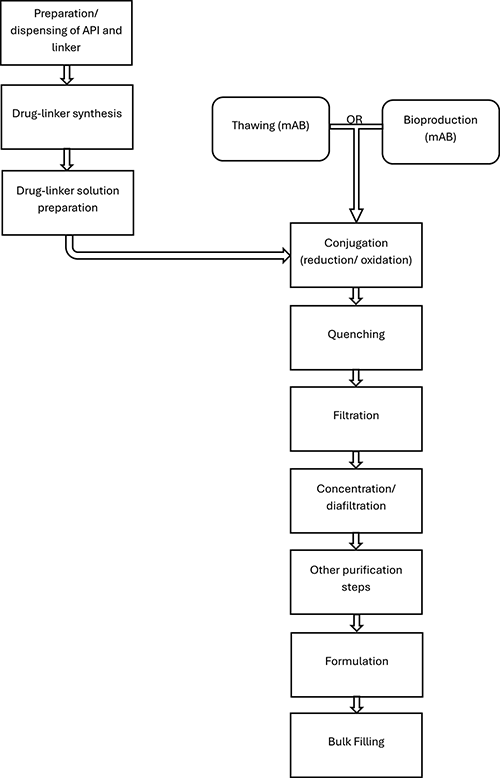
Containment in ADC Facilities / Containment Evaluation and Design Considerations · Virgilio P · Howorth Air Technology
Containment API Evaluation Dispersion Antibody drug conjugate The containment of hazardous substances is a critical aspect of pharmaceutical manufacturing, particularly in facilities handling antibody drug conjugates (ADC). This article explores the principles, evaluation methods, and design considerations for process containment systems, with a focus on ADC production environments. All the information is based on the experience of high containment process design projects in which the author and his workgroup have participated in the last years. Containment isolator design must comply with several European directives and standards. The following is a selection of the most relevant: Annex 1 ("Manufacture of Sterile Medicinal ...
-

Neue Lösung zum Konditionieren hochtoxischer APIs unter Reinraumbedingungen
(Treffer aus Tech4Pharma, Nr. 01, Seite 15 (2026))
Neue Lösung zum Konditionieren hochtoxischer APIs unter Reinraumbedingungen / Content Marketing
Biopharmazeutische Active Pharmaceutical Ingredients (APIs) sind hochpotent. Ihre Herstellung erfordert einen besonderen Schutz der Mitarbeiter und häufig eine Klimakonditionierung des Produkts. Weiss Pharmatechnik hat dafür einen Isolator mit einem Klimaschrank als geschlossenes System zu einem Reinraum kombiniert. APIs bieten zahlreiche innovative Möglichkeiten zur Behandlung komplexer Krankheiten wie Epilepsie, Depressionen und Alzheimer. Sie besitzen die Fähigkeit, zielgerichtet auf das Immunsystem einzuwirken. Der Umgang mit bioaktiven Wirkstoffen erfordert deshalb Schutzmaßnahmen für Mitarbeiter und Umwelt. Auch das Produkt selbst muss geschützt werden, da Umgebungsparameter wie Feuchte und Temperatur die Eigenschaften der Wirkstoffe erheblich beeinflussen können. Die Verarbeitungsschritte sind daher sehr komplex. Das Containment-Klimakammer-System ... -

Umbruch und Aufbruch
Rubrik: Gastkommentar
(Treffer aus pharmind, Nr. 01, Seite 15 (2026))
Umbruch und Aufbruch / Klinische Forschung wettbewerbsfähig und innovativ gestalten*Bericht über das 33. Symposium des Bundesverbands Medizinischer Auftragsinstitute (BVMA) e. V. am 21. Nov. 2025 · Hammer A, Karl A · Winicker Norimed und BVMA
Studienstandort Deutschland Medizinforschungsgesetz KI Klinische Forschung Forschungsdatennutzung Moderiert von Katrin Schmiedl und Robert Krausche, startete nach der Einführung die erste Vortragsreihe des Tages zum Thema Regulatorik. Prof. Dr. Jens Peters, Geschäftsfeldleiter Klinische Forschung beim Bundesverband der Pharmazeutischen Industrie (BPI), eröffnete mit einem umfassenden Überblick zu regulatorischen Entwicklungen in der EU. Zentrales Thema war das Ende der 3-jährigen Übergangsphase der Clinical Trials Regulation (CTR): Seit Einführung der Pflicht zur Nutzung des Clinical Trials Information System (CTIS) wurden durchschnittlich 200 neue Studien pro Monat eingereicht, davon rund 80 multinationale Prüfungen. Nicht umgestellte Studien gelten seit 31. Jan. 2025 als nicht konform. Prof. Dr. Peters stellte ...
-
Der neue SMEPAC-Leitfaden
Rubrik: Reinraum
(Treffer aus Tech4Pharma, Nr. 01, Seite 16 (2026))
Nicolai R | Schöler M | Bockius B | Gottlieb O
Der neue SMEPAC-Leitfaden / Die Verifizierung der Leistung von Containment-Systemen · Nicolai R, Schöler M, Bockius B, Gottlieb O · F. Hoffmann – La Roche und Fette Compacting und Merck Electronics und PharmaCon Service
Containment Expositionsmessung Arbeitshygiene Hochaktiv Wirkstoffherstellung In der pharmazeutischen Industrie mit ihrem stark regulierten Umfeld sind Containment-Systeme allgegenwärtig. Häufig werden diese Systeme ausschließlich mit dem Schutz der Produkte vor äußeren Einflüssen in Verbindung gebracht. So ist z. B. der Begriff „Reinraum“ ein Synonym für ein Containment zum Schutz der Produkte durch Kontamination von außen. Containment-Spezialisten sprechen hierbei von einem sekundären Containment. Produkte wurden (und werden z. T. immer noch) in diesen sekundären Containments (Reinräumen) oft offen gehandhabt – die Substanzen sind den Umgebungsbedingungen des Reinraums ohne weitere Barriere ausgesetzt. Daher müssen diese Reinräume je nach Anforderung des Produkts eine definierte Reinheit aufweisen, welche ...
-

PRAC – News
Rubrik: Ausschüsse
(Treffer aus pharmind, Nr. 01, Seite 20 (2026))
PRAC – News / Empfehlungen zum Risikomanagement für Humanarzneimittel im Nov. 2025 · Thurisch B, Sickmüller B · Bundesverband der Pharmazeutischen Industrie
Humanarzneimittel Referral-Verfahren Arzneimittelsicherheit Pharmakovigilanz Arzneimittelrisiken Der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (Pharmacovigilance Risk Assessment Committee, PRAC) ist in erster Linie für die Beurteilung aller Aspekte des Risikomanagements von Humanarzneimitteln zuständig. Dies umfasst die Ermittlung, Bewertung, Minimierung und Kommunikation der Risiken von Nebenwirkungen, unter gebührender Berücksichtigung des therapeutischen Nutzens des Humanarzneimittels, der Gestaltung und Bewertung der Unbedenklichkeitsstudien nach der Genehmigung sowie Pharmakovigilanz-Audits. Der PRAC gibt somit – abhängig vom jeweiligen Verfahren – Empfehlungen an den Ausschuss für Humanarzneimittel (Committee for Medicinal Products for Human Use, CHMP), die Koordinierungsgruppe (Coordination Group for Mutual Recognition and Decentralised Procedures – human, CMDh), ...
-

G-BA und IQWiG – News
Rubrik: Ausschüsse
(Treffer aus pharmind, Nr. 01, Seite 20 (2026))
G-BA und IQWiG – News / Bewertungen und Beschlüsse von Dez. 2025 · Wilken M, Lietz C · Bundesverband der Pharmazeutischen Industrie
G-BA IQWiG Arzneimittelbewertung Zusatznutzen Stellungnahmeverfahren Beschlüsse des G-BA vom 16. Okt. 2025 zur Änderung der Arzneimittel-Richtlinie (AM-RL) in Anlage XII (Verfahren nach § 35a SGB V): Nivolumab (neues Anwendungsgebiet: nicht kleinzelliges Lungenkarzinom, PD-L1-Expression ≥ 1 %, neoadjuvante und adjuvante Therapie, Monotherapie oder Kombination mit platinbasierter Chemotherapie) Für den Wirkstoff Nivolumab (Opdivo®) hat das Bewertungsverfahren für ein neues Anwendungsgebiet am 15. Juni 2025 begonnen. Als zweckmäßige Vergleichstherapie (zVT) wurde vom G-BA für die neoadjuvante Behandlung Pembrolizumab in Kombination mit einer platinbasierten Therapie und für die adjuvante Behandlung Pembrolizumab festgelegt. Dieser Festlegung ist der pharmazeutische Unternehmer (pU) gefolgt. Durch die vom IQWiG durchgeführte Überprüfung der Vollständigkeit des Studienpools wurde ...
-

COMP – News
Rubrik: Ausschüsse
(Treffer aus pharmind, Nr. 01, Seite 20 (2026))
COMP – News / Empfehlungen zu Orphan-Arzneimitteln im Okt. 2025 · Throm S
Humanarzneimittel Orphan Drugs Seltene Krankheiten Zuerkennungsverfahren Orphan-Zulassungen Der Ausschuss für Arzneimittel gegen seltene Krankheiten (Committee for Orphan Medicinal Products, COMP) verabschiedete bei seiner Sitzung vom 7.–8. Okt. 2025 bei der Europäischen Arzneimittel-Agentur (EMA) in Amsterdam folgende Voten: 13 Empfehlungen für die Zuerkennung des Orphan-Status für die folgenden in Entwicklung befindlichen Medikamente: N-(6-Amino-5-ethylpyridin-3-yl)-2-((2R,5S)-5-methyl-2-(2-(1-methylpiperidin-4-yl)benzo[d]thiazol-5-yl)piperidin-1-yl)-2-oxoacetamid zur Behandlung von Pankreaskarzinomen; 98 780 Betroffene; PPD Bulgaria Leuconostic citreum Stamm G511 zur Behandlung der primären sklerosierenden Cholangitis; 89 800 Betroffene; Harvest Integrated Research Organization Nangibotid zur Behandlung der Sichelzellerkrankung; 71 840 Betroffene; Inotrem 2-(3-Chlorphenyl)-N-[6-(trifluormethyl)-1,3-benzothiazol-2-yl]acetamid zur Behandlung der amyotrophen Lateralsklerose; 44 900 Betroffene; Molefy Pharma Surovatamig zur Behandlung von B-lymphatischen Leukämien und ...
-

CHMP und CMDh – News
Rubrik: Ausschüsse
(Treffer aus pharmind, Nr. 01, Seite 20 (2026))
CHMP und CMDh – News / Empfehlungen zu Humanarzneimitteln im Dez. 2025 · Throm S
Opinions Arzneimittelzulassung Pharmakovigilanz Anerkennungsverfahren Wissenschaftliche Beratung Bei der Sitzung des Ausschusses für Humanarzneimittel (CHMP) vom 8.–11. Dez. 2025 bei der Europäischen Arzneimittel-Agentur (EMA) in Amsterdam wurden folgende Ergebnisse erzielt: Der CHMP verabschiedete: 5 positive Voten für folgende Medikamente mit neuem Wirkstoff: Aumseqa® (Aumolertinib) : Filmtabletten von SFL Pharmaceuticals zur Erstlinientherapie Erwachsener mit fortgeschrittenen nicht kleinzelligen Lungenkarzinomen mit EGFR-Exon-19-Deletionen oder Exon-21(L858R)-Substitutionsmutationen sowie zur Behandlung Erwachsener mit fortgeschrittenen EGFR T790M Mutations-positiven nicht kleinzelligen Lungenkarzinomen. Der Wirkstoff gehört zu den EGFR-Tyrosinkinase-Inhibitoren (Anatomischer-Therapeutischer-Chemischer[ATC]-Code: L01EB11). Aumseqa hemmt irreversibel EGFR mit den sensitierenden Mutationen EGFR-Exon-19-Deletion und L858R sowie mit EGFR-Resistenzmutation (EGFR T790M). Der Nutzen von Aumseqa besteht ...
Sie sehen Artikel 11921 bis 11930 von insgesamt 11999
- Erste Seite
- 1191
- 1192
- 1193
- 1194
- 1195
- Letzte Seite