Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12078 Beiträge für Sie gefunden
-

Etikettendrucker
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 255 (2019))
Etikettendrucker / Produkte
TSC *) stellt die neuen Thermotransferdrucker ML240P und ML340P vor. Diese Industrie-Etikettendrucker wurden signifikant in den Abmessungen verschlankt. Die Kombination aus Druckguss-Gehäuse, modularem Aufbau und moderner Drucktechnologie ermöglicht einen dauerhaft stabilen, geräuscharmen und zugleich effizienten Betrieb. Für optimale Druckergebnisse auf unterschiedlichsten Etikettenmaterialien sorgen dabei der justierbare Thermodruckkopf und das Selbstdiagnose-Tool TPH Care. Der ML240P ist mit einer Druckauflösung von 203 dpi, der ML340P mit 300 dpi erhältlich. Beide Modelle besitzen ein 2,3“-Farbdisplay mit personalisierbarer Bedienerführung und 6 Bedientasten. Durch die komplett hochklappbare Abdeckung können Materialwechsel schnell durchgeführt werden. Der Druckmechanismus ermöglicht den werkzeuglosen und daher ebenso zügigen Austausch von Druckkopf und Druckplattenwalze ... -

Temperaturkalibratoren
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 255 (2019))
Temperaturkalibratoren / Produkte
Bislang waren die zukunftsweisenden Vorteile der TP Premium Temperaturkalibratoren nur in Geräten mit Temperaturbereichen von –55 °C bis maximal 255 °C erhältlich. Mit dem TP 37450E.2 dringt SIKA *) nun in neue Temperaturbereiche vor, natürlich nicht ohne den Markt mit weiteren, neuen Eigenschaften aufzurütteln. Während typische Grenztemperaturbereiche bei Marktbegleitern bislang bei 350 °C lagen, erreicht SIKA mit dem TP 37450E.2 problemlos 450 °C und das bei einem Kalibriervolumen von durchschnittlich 60x150 mm. Für den Anwender bedeutet das eine klare Zeitersparnis. Er kann eine große Anzahl von Prüflingen gleichzeitig in dem großen Kalibriervolumen kalibrieren. Einzigartig bei mobilen Temperaturkalibratoren ist zudem das revolutionäre, neue Lüftersystem, das erstmals ... -

Ausblasmaschinen
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 254 (2019))
Ausblasmaschinen / Produkte
Groninger *) hat eine neue Ausblasmaschine im Produktportfolio. Die FlexClean vereint mehr Flexibilität, mehr Qualität und mehr Leistung. Die Anlage ist oval ausgelegt. Das heißt, die Zeitspanne, in der sich die Flaschen kopfüber in der Transportvorrichtung befinden und ausgeblasen werden, ist wesentlich länger als bei einem runden Umlauf. Dadurch ist die Wahrscheinlichkeit, dass Schmutzpartikel in den Flaschen zurückbleiben, geringer. Das Maschinenkonzept ermöglicht zudem einen höheren Grad an Flexibilität: Auf den Grundhaltern können unterschiedliche Transportträger platziert werden. In kleinen Formatbereichen, in denen häufig hohe Leistungen gefordert werden, können so pro Träger 3 Objekte gleichzeitig ausgeblasen werden. Bei großen Formaten erfolgt das ... -

Sammelpacker
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 254 (2019))
Sammelpacker / Produkte
Romaco *) hat die Tertiärverpackungslösung Promatic PAK 130 entwickelt. Der halbautomatische Sammelpacker eignet sich ideal für die sichere Aggregation von Arzneimittelpackungen nach der Serialisierung. Der Sammelpacker verpackt Faltschachteln in Versandkartons und erfüllt höchste Standards bei der Produktion fälschungssicherer Pharmaverpackungen. Hierzu ist die Maschine für eine Anbindung an Softwarelösungen konzipiert, die eine sichere Aggregation ermöglichen. Die Wahl des Systems zur Aggregation erfolgt durch den Pharmahersteller selbst – Romaco Promatic konfiguriert den PAK 130 dann entsprechend. Nach der Serialisierung der Sekundärverpackungen übernimmt dieser die Aggregation bei der Verpackung der Faltschachteln in Versandkartons. Damit wird der Originalitätsnachweis sowohl für die Sekundär- als auch die ... -

Dispenser
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 254 (2019))
Dispenser / Produkte
ViscoTec *) erweitert mit dem Pharmadispenser 4VPHD6 die VPHD-Dispenser-Serie im GMP-Design um ein Gerät für kleine Mengen. Es ist jetzt möglich, Kleinstmengen von 0,1 ml abzufüllen bzw. ab 0,2 ml pro Minute kontinuierlich zu dosieren. Der neue 4-stufige Dispenser ermöglicht durch eine zusätzliche Stufe das Dosieren bei einem Gegendruck von > 20 bar. Das kann z. B. beim Einspritzen in HPLC-Anlagen erforderlich sein oder auch beim kontinuierlichen Dosieren eines Wirkstoffs in einen Extruder. Die Abfüllung bestimmter Pharmazeutika ist herausfordernd für die Dosiertechnologie. Dazu gehören etwa quervernetzte Hyaluronsäure, schersensitive Zwischenprodukte wie proteinbeladene Lösungen, partikelbeladene, abrasive Pasten und hochpotente Wirkstoffe. Ein gleichbleibender Fadenabriss dank programmierbarem Rückzug garantiert ... -

Massenspektrometer
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 253 (2019))
Massenspektrometer / Produkte
Shimadzu *) hat sein Angebot an MALDI-MS-Systemen um das neue MALDI-8020 erweitert. Es eignet sich für die Qualitätskontrolle in der Pharmazeutik sowie für Forschungs- und Auftragslabore in Wissenschaft und Industrien. Konkrete Anwendungen sind etwa die Analyse von Proteinen/Peptiden, Lipiden, Kohlenhydraten in der Life-Science-Analytik oder Qualitäts- und Synthesekontrollen von Polymeren. Die sehr einfache Gerätebedienung durch die anwenderfreundliche MALDI-Solutions-Software unterstützt die große Zahl an Applikationen. Sie ist intuitiv bedienbar, bietet Sicherheitsmerkmale, unterstützt Audit Trails und Nutzermanagement. Die Nutzerschnittstelle macht sie leicht erlernbar, sodass selbst Anfänger in der Massenspektrometrie direkten Zugang zum System haben. Weitere Zusatzsoftwares stehen den Anwendern bei den verschiedensten ... -

Etikettieranlagen
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 253 (2019))
Etikettieranlagen / Produkte
Bluhm Systeme *) hat die neue Etikettieranlage Geset 314 mit Orbiter entwickelt. Ovale oder konische Verpackungen werden herkömmlicherweise während des Kennzeichnungsprozesses von einem Grund- und Kopfband fixiert. Mit sehr hoher Etikettiergenauigkeit wischt die Etikettieranlage dabei Vorder- und Rückseitenetiketten auf die Produkte auf. Um eine noch präzisere Etikettierung zu realisieren, wurde die Geset 314 zusätzlich zum Grund- und Kopfband mit einem sog. Orbiter-Modul versehen. Die Greifer dieses Orbiters entsprechen jeweils exakt der Negativform der individuellen Produkte. Unmittelbar vor der Etikettierung erfasst und umschließt das Modul das heraneilende Gebinde und bewirkt dank seines individuellen Formats dessen perfekte Ausrichtung. In der Folge werden die ... -

Palettenetikettierer
Rubrik: Produkte
(Treffer aus TechnoPharm, Nr. 04, Seite 253 (2019))
Palettenetikettierer / Produkte
Mit Aluminium- oder Edelstahlgehäuse, links- oder rechtshändiger Konfiguration, verschiedenen Klimakits für den Einsatz unter besonders schwierigen Umgebungsbedingungen sowie einem integrierten Kontrollscanner und farbigem Touch-Panel lässt sich der Palettenetikettierer M230i von Domino *) einfach für spezifische Kundenbedürfnisse konfigurieren. Der flexible Palettenetikettierer ist kompakt, robust, einfach integrierbar und sowohl für neue Anlagen als auch für die Integration in bestehende Fertigungslinien geeignet. Er gewährleistet eine vollständige Lieferkettenkonformität gemäß GS1-Standard. Mit QuickPal, der Softwarelösung für die Systemintegration der Palettenetikettierung, ist die Steuerungsanbindung eines Palettenetikettiersystems an das jeweilige Kundensystem unkompliziert realisierbar. -

30 Jahre METTLER TOLEDO PCE
Rubrik: Spektrum
(Treffer aus TechnoPharm, Nr. 04, Seite 252 (2019))
30 Jahre METTLER TOLEDO PCE / Spektrum
Was 1989 im südhessischen Bickenbach als 2-Personen-Unternehmen begann, gehört 30 Jahre später zu einem Weltkonzern: Heute zählt METTLER TOLEDO PCE zu den führenden Anbietern für Track & Trace-Lösungen und visuelle Produktinspektion in der Pharmaindustrie. Seit der Gründung nimmt die Pharmacontrol Electronic GmbH (PCE) eine technologische Vorreiterrolle ein. Zu den ersten Eigenentwicklungen zählten Codeleser zur Kontrolle von Faltschachteln und Beipackzetteln sowie Farbkamerasysteme zur Blisterfüllgutkontrolle. 1995 führte das Unternehmen mit Smart Kameras eine leistungsstarke und intelligente Aufnahmetechnologie für die Produktinspektion ein. Diese Technologie bildet bis heute den Grundstein für komplexe und vernetzte Kontrollszenarien, wie sie etwa bei der Pharmaserialisierung und -aggregation nötig sind. ... -
AVionics – von Big Data zu Smart Data
Rubrik: Spektrum
(Treffer aus TechnoPharm, Nr. 04, Seite 250 (2019))
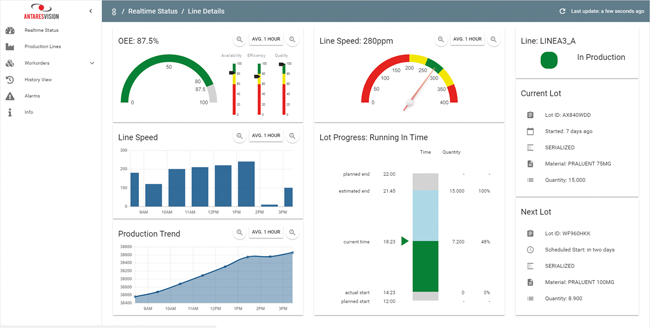
AVionics – von Big Data zu Smart Data / Spektrum
Nachdem viele Unternehmen die Implementierung der Serialisierung abgeschlossen haben und somit den EU-Vorschriften zu gefälschten Arzneimitteln (EU Falsified Medicines Directive) gefolgt sind, ist es nun an der Zeit, die getätigte Investition zu nutzen. Die Daten, welche bei der Serialisierung erhoben werden, sind auszuwerten und zu optimieren. Durch die in Unternehmen geforderten Softwaresysteme, welche die Automatisierung von Produktionslinien steuern, wurden neue Wege in der Datengewinnung und -verwaltung eröffnet. Dank der Expertise von Antares Vision in der Umsetzung von Lösungen entwickelte das italienische Unternehmen innovative Wege zur Erfassung und Verarbeitung von Daten, um so den Mehrwert für jedes einzelne Unternehmen zu generieren. ...
Sie sehen Artikel 3301 bis 3310 von insgesamt 12078
- Erste Seite
- 329
- 330
- 331
- 332
- 333
- Letzte Seite