Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12078 Beiträge für Sie gefunden
-

Pharma Aldenhoven
Rubrik: Sonderteil CPhI 2019
(Treffer aus TechnoPharm, Nr. 05, Seite 314 (2019))
Pharma Aldenhoven / CPhI 2019
Pharma Aldenhoven GmbH & Co. KG *) wurde im Juni 1997 gegründet und ist seither Ihr Lohnhersteller für die richtige Lösung. Als ein marktführender Auftragshersteller sind wir spezialisiert auf die kostengünstige Entwicklung, Herstellung und Konfektionierung nach GMP-Richtlinien in den Kategorien Arzneimittel, Medizinprodukte, Nahrungsergänzungsmittel und Kosmetika. Wir bieten u. a. Nasen-, Ohren- und Rachensprays Bi-Phase-Trinkampullen Salben, Gele, Cremes Säfte, Sirupe, Suspensionen, Tonika, Tropfen Bäder Einreibungen Konfektionierung fester Formen Außerdem bieten wir ein umfangreiches Portfolio an eigenen Zulassungen zum Mitvertrieb, Instrumenteller Analytik (z. B. HPLC, GC, DC, IR) und Stabilitätseinlagerungen nach ICH. Herstellungserlaubnis nach § 13 AMG DIN EN ISO 13485:2016 IFS Food, Version 6.1 (International Food Standard) -

Hoffmann Neopac
Rubrik: Sonderteil CPhI 2019
(Treffer aus TechnoPharm, Nr. 05, Seite 314 (2019))
Hoffmann Neopac / CPhI 2019
Hoffmann Neopac *) ist ein privat geführtes Unternehmen mit Hauptsitz in Thun, Schweiz. Die Gruppe produziert an sechs Standorten hochwertige Verpackungen aus Metall und Kunststoff: HOFFMANN-Dosen in der Schweiz und in Holland. Polyfoil®- und Kunststofftuben bei NEOPAC in der Schweiz, in Ungarn und in den USA sowie bei 3D Neopac in Indien. Zu den langjährigen Kunden gehören international tätige Pharma-, Kosmetik- und Konsumgüterhersteller in den Märkten Europa, Nordamerika und Asien. Mit der neu eröffneten Produktionsstätte in den USA beschäftigt Neopac rund 1 250 Mitarbeiter und verfügt über eine Kapazität von 1,3 Mrd. Tuben. Das Unternehmen legt großen Wert auf die Nachhaltigkeit seiner ... -
CPhI 2019
Rubrik: Sonderteil CPhI 2019
(Treffer aus TechnoPharm, Nr. 05, Seite 312 (2019))
CPhI 2019 / CPhI 2019
Die CPhI worldwide findet vom 05.–07. Nov. 2019 in Frankfurt statt. In diesem Jahr feiert die Veranstaltung ihren 30. Geburtstag. Dabei werden etwa 45 000 Besucher und 2 500 Aussteller erwartet. Einen guten, ersten Überblick zu den zahlreichen Events und Vorträgen bietet der CPhI worldwide Event Preview Guide 2019, der unter www.cphi.com verfügbar ist. Die Messe bündelt verschiedene Bereiche des Pharmamarkts unter einem Dach und bietet Ausstellern und Besuchern vielfältige Möglichkeiten: Erweiterung des eigenen Netzwerks Schließung neuer Geschäftspartnerschaften Treffen mit internationalen Kunden und Auftraggebern Informationen über die neusten Trends in der Pharmabranche In der InnoPack-Halle 11.1 (Stand: 111G10 des ECV ... -
GMP-konforme Selbstkalibrierung von Temperaturmessstellen
Rubrik: Messen/Steuern/Regeln
(Treffer aus TechnoPharm, Nr. 05, Seite 304 (2019))
GMP-konforme Selbstkalibrierung von Temperaturmessstellen / Eine Bestandsaufnahme · Garbers P · Endress+Hauser Messtechnik GmbH+Co.KG, Weil am Rhein
Selbstkalibrierung Datenintegration GMP Curie-Temperatur Die operative Kalibrierung und langfristige Kalibrierplanung in den mitteleuropäischen pharmazeutischen Unternehmen befinden sich seit einigen Jahren im Wandel. Dies hat seinen Ursprung im Spannungsfeld zwischen Compliance, Innovation und Kostendruck. Im internationalen Wettbewerb wird die maximale Anlagenauslastung bzw. Anlagenverfügbarkeit zunehmend zum Hauptziel der produzierenden Unternehmen. Für das Wartungs- und Kalibrierpersonal ergeben sich daraus neue Anforderungen, denn gleichzeitig besteht der Anspruch, Inspektionen weiterhin ohne Beanstandungen zu bestehen. Weltweit gibt es hier immer noch Nachholbedarf, denn knapp 5 % der Warning Letter der U.S. Food and Drug Administration (FDA) der Jahre 2013–2017 behandelten Mängel in der Kalibrierung. Im Bereich Wartungsmängel ...
-
Bauelemente für den Reinraumbau: Wand- und Deckensysteme
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 298 (2019))
Bauelemente für den Reinraumbau: Wand- und Deckensysteme / Flechl • Wand- und Deckensysteme · Flechl H · Freiberuflicher Fachautor, Wien (Österreich)
Reinraum Decken- und Wandsysteme Wandverkleidungen Beschichtungen Deckenplatten Wie ist der heutige Stand der Technik bei Decken- und Wandsystemen? Was kann der Nutzer heute von kompetenten und erfahrenen Lieferanten verlangen? Auf welche Unterschiede ist bei der Bewertung von Angeboten und Alternativen bei den ausgewählten Anbietern zu achten? Die Checkliste in Tab. 1 soll hierbei Hilfestellung leisten. Checkliste Wand- und Deckensysteme erfüllt? Beurteilungskriterium ja nein n. a. ausgereifte/bewährte Konstruktion prüfbare Dichtheit, sofern gefordert definierte Baustoffklasse nach behördlicher oder eigener Vorgabe für Brandabschnitte oder den Anforderungen des Versicherers entsprechende Feuerwiderstandsklasse Größe/Rasterung der Elemente: Achsraster, Bandraster, Monoblock; änderungsfreundlich, ergänzungsfreundlich und leicht demontierbar gut durchkonstruierte Anschlüsse Wand-Wand, ...
-
Etablierung eines GMP-Monitoringkonzeptes im pharmazeutischen Herstellbereich
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 286 (2019))
Etablierung eines GMP-Monitoringkonzeptes im pharmazeutischen Herstellbereich / Wickert und Büßing • Etablierung eines GMP-Monitoringkonzeptes · Wickert M, Büßing W · Testo Industrial Services GmbH, Kirchzarten und Boehringer Ingelheim Pharma GmbH & Co. KG, Ingelheim
Qualifizierung Pharma Qualifizierung Versorgungstechnische Anlagen Monitoring Mapping Die Zentralisierung der Prozessentwicklung der Boehringer Ingelheim Vetmedica GmbH (BIV), welche zuvor auf 4 Gebäude verteilt war, stellte die Grundlage des Neubauprojektes „Laborgebäude mit Herstellbereich“ zur Etablierung eines GMP-Monitoringkonzeptes für die Betriebsphase dar. Durch die Erweiterung des „Laborgebäudes Chemie“ am Standort Ingelheim konnte zudem ein Insourcing der Produktion im Entwicklungsmaßstab erfolgen. Nachdem der Spatenstich Ende Juni 2012 stattgefunden hatte, konnten im Frühjahr 2014 die ersten Räume genutzt und ab Sommer 2014 die Herstellbereiche im Erdgeschoss bezogen werden. Da es sich hierbei um Good-Manufacturing-Practice(GMP)-Bereiche handelt, die einer Reinraum-Klasse D (RRK D) zugeordnet sind, musste zunächst eine Qualifizierung durchgeführt werden. Im ...
-
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 278 (2019))
Wagner B | Brinz T | Otterbach S
Quality by Design für Kapselfüllprozesse mittels innovativer pharmazeutischer Prozessvalidierung / Teil 1 · Wagner B, Brinz T, Otterbach S · Bosch Packaging Technology GmbH, Waiblingen
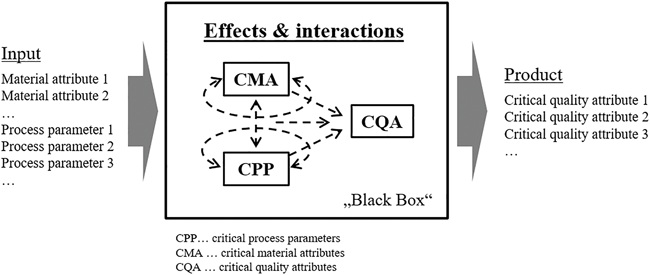
Quality by Design (QbD) Capsule Filling Process Development Design of Experiment (DoE) Powder Filling Ein detailliertes Prozessverständnis ist für die Validierung eines Prozesses unumgänglich. Mit dem Begriff Quality by Design (QbD) setzte die U.S. Food and Drug Administration (FDA) ein Paradigma für die pharmazeutische Prozessentwicklung [1]. Bekannt aus anderen Industrien (etwa Automobil) beschreibt QbD die Idee, dass Qualität nicht erst nachträglich im Produkt getestet wird, sondern bereits bei der Planung und Entwicklung eines Prozesses entsteht. Voraussetzung: Alle entscheidenden Einflüsse auf das Arzneimittel und den Produktionsprozess sowie deren Wechselwirkungen untereinander sind bekannt, und diese können auch gesteuert oder kontrolliert werden. Dann ...
-
Technologie-Transfer von pharmazeutischen Prozessen
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 270 (2019))
Technologie-Transfer von pharmazeutischen Prozessen / Gottlieb • Technologie-Transfer · Gottlieb O · NNE A/S, Virum (Dänemark)
Technologie-Transfer Pharmazeutische Industrie Launch-Plant-to Large-Scale-Produktion F&E/R&D-to-launch-plant-Produktion In der pharmazeutischen Industrie werden Produkte oft an mehr als nur einem Standort hergestellt, um eine Lieferung an den Kunden zu garantieren. Wird z. B. ein Produkt neu auf den Markt gebracht oder in einer zusätzlichen Produktionsstätte hergestellt, ist eine Übertragung des Produktionsprozesses nötig. Hierbei ist insbesondere darauf zu achten, dass mögliche neue regulative Anforderungen berücksichtigt werden, die etwa erfordern, dass Produkte für den lokalen Markt auch in dem entsprechenden Land oder der Region hergestellt werden müssen. Eine solche Regelung haben u. a. Russland und China. Der Prozess des Überführens eines Produktes oder eines ganzen Produktportfolios ...
-
Prozessentwicklung für Gentherapie-Produkte
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 05, Seite 262 (2019))
Bergheim-Pietza S | Raghavan B | Collins M | Walls S | Lambropoulos A | Sievers D
Prozessentwicklung für Gentherapie-Produkte / Optimierung der Klärungsfiltration von Zellkulturen mit viralen Vektoren · Bergheim-Pietza S, Raghavan B, Collins M, Walls S, Lambropoulos A, Sievers D · Pall Biotech, Dreieich und
Gentherapie Virale Vektoren Zellkulturernte Zellkulturfiltration Virusfiltration In der Gentherapie werden genmodifizierende Technologien genutzt, um beschädigte körpereigene Zellen zu reparieren, zu korrigieren oder zu ersetzen. Es wird sowohl mit adhärenten, auf Oberflächen wachsenden Zellen als auch mit nicht-adhärenten Suspensionszellen produziert. Lentiviren und adeno-assoziierte Viren (AAV) stehen derzeit im Fokus der Forschung und sind aufgrund ihrer Eigenschaften die meistverbreiteten Vektoren. Nach Jahren der Forschung entwächst die Gentherapie langsam den Kinderschuhen. Mehr und mehr Gentherapeutika werden zugelassen. In der Folge steigt die Notwendigkeit, nicht nur funktionelle Produkte herzustellen, sondern diese auch in ausreichender Menge und wirtschaftlich zu produzieren. Folgerichtig konzentriert sich die Prozessentwicklung ...
-

Aufwachen, Papa Staat!
Rubrik: Editorial
(Treffer aus TechnoPharm, Nr. 05, Seite 257 (2019))
Aufwachen, Papa Staat! / Editorial
Sehr geehrte Leser des TechnoPharm-Journals, die umweltfreundlichste Energie ist immer noch diejenige, die gar nicht erst gebraucht wird. Folgerichtig ist der Energieeffizienz-Index EEI des Instituts für Energieeffizienz in der Produktion (EEP) der Universität Stuttgart zum Winter 2018/19 so hoch wie noch nie – auch die Pharmaindustrie möchte also ihre Energieeffizienzmaßnahmen intensivieren. Der EEI entsteht in Zusammenarbeit mit der Deutschen Energie-Agentur (dena), dem Bundesverband der Deutschen Industrie (BDI), dem Fraunhofer IPA, dem TÜV Rheinland u. a. Dabei gilt jedoch: Vorsicht ist die Mutter der Porzellankiste! Dies scheint zumindest die Tatsache anzudeuten, dass zwei Drittel der befragten Pharmaunternehmen die Bedeutung der Energieeffizienz in ...
Sie sehen Artikel 3261 bis 3270 von insgesamt 12078
- Erste Seite
- 325
- 326
- 327
- 328
- 329
- Letzte Seite